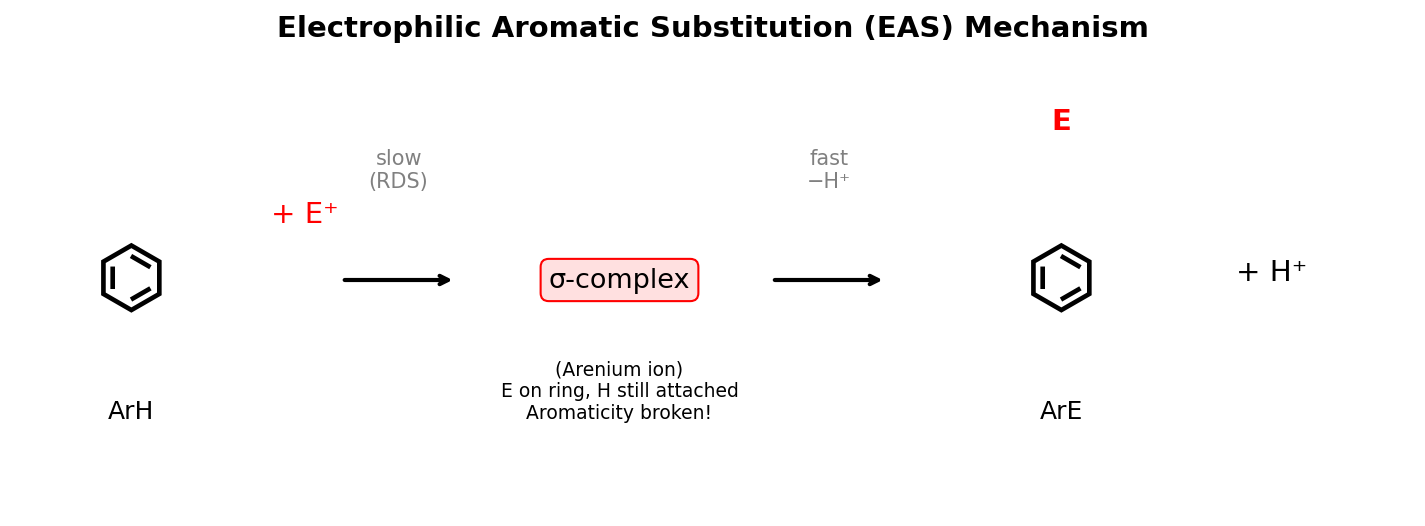
① 生成亲电试剂 E+
② E+ 进攻苯环π电子 → 形成σ络合物(Wheland中间体,芳香性被破坏)
③ σ络合物失去H+ → 恢复芳香性,得到取代产物
苯的分子式:C6H6,不饱和度 = 4(3个双键 + 1个环)
| 体系 | π电子数 | 4n+2? | 判断 |
|---|---|---|---|
| 苯 | 6 | n=1 ✓ | 芳香 |
| 环丁二烯 | 4 | 4n(n=1) ✗ | 反芳香 |
| 环辛四烯 | 8 | 4n(n=2) ✗ | 非平面→非芳香 |
| 环戊二烯− | 6 | n=1 ✓ | 芳香 |
| 环庚三烯+ | 6 | n=1 ✓ | 芳香 |
| 环丙烯+ | 2 | n=0 ✓ | 芳香 |
| 环丙烯− | 4 | 4n(n=1) ✗ | 反芳香 |
| [10]轮烯 | 10 | n=2 ✓ | 需共平面才芳香 |
| [14]轮烯 | 14 | n=3 ✓ | 芳香 |
| [18]轮烯 | 18 | n=4 ✓ | 芳香 |
简单取代基直接命名:甲苯、氯苯、硝基苯、苯酚、苯胺、苯甲酸、苯甲醛等
| 位置关系 | 前缀 | 编号 | 示例 |
|---|---|---|---|
| 1,2- | 邻(ortho-, o-) | 相邻 | 邻二甲苯 |
| 1,3- | 间(meta-, m-) | 间隔一个 | 间二甲苯 |
| 1,4- | 对(para-, p-) | 对面 | 对二甲苯 |
① 生成亲电试剂 E+
② E+ 进攻苯环π电子 → 形成σ络合物(Wheland中间体,芳香性被破坏)
③ σ络合物失去H+ → 恢复芳香性,得到取代产物

| 反应 | 试剂/条件 | 亲电试剂E+ | 产物 | 要点 |
|---|---|---|---|---|
| 硝化 | 浓HNO3/浓H2SO4 | NO2+ | ArNO2 | 混酸,温度控制 |
| 卤代 | Br2(Cl2)/FeBr3(FeCl3) | Br+(Cl+) | ArBr(ArCl) | 必须Lewis酸催化 |
| 磺化 | 发烟H2SO4(含SO3) | SO3 | ArSO3H | 可逆反应! |
| F-C烷基化 | RCl/AlCl3 | R+ | ArR | 会重排+多取代 |
| F-C酰基化 | RCOCl/AlCl3 | RCO+ | ArCOR | 不重排,一元取代 |
HNO3 + 2H2SO4 → NO2+ + H3O+ + 2HSO4−
Br2 + FeBr3 → Br+·FeBr4−(极化产生亲电性Br)
最后:FeBr4− + H+ → FeBr3 + HBr(催化剂再生)
苯 + HCHO + HCl,ZnCl2催化,60°C → C6H5CH2Cl(苄氯/氯化苄)
活化+邻对位:−NH2, −NHR, −NR2, −OH, −OR, −NHCOR, −OCOCH3, −R, −C6H5
特征:与苯环直接相连的原子上有孤对电子或提供电子的σ键,能通过共振效应(+C)或超共轭向环供电子
−F, −Cl, −Br, −I
吸电子诱导效应(−I) > 供电子共振效应(+C) → 总体钝化
但共振效应决定位置 → 邻对位定位
钝化+间位:−NO2, −CF3, −CN, −SO3H, −CHO, −COR, −COOH, −COOR, −CONH2
特征:与苯环直接相连的原子含有多重键(双键或三键连接电负性原子),强吸电子
| 类别 | 取代基 | 活化/钝化强度 | 定位 |
|---|---|---|---|
| 邻对位定位基 (活化) | −NH2, −NHR, −NR2 | 强活化 | 邻/对位 |
| −OH, −O− | 强活化 | 邻/对位 | |
| −OR, −OCOR | 中等活化 | 邻/对位 | |
| −NHCOR | 中等活化 | 邻/对位 | |
| −R, −C6H5 | 弱活化 | 邻/对位 | |
| 邻对位定位基 (钝化,卤素) | −F | 弱钝化 | 邻/对位 |
| −Cl | 弱钝化 | 邻/对位 | |
| −Br | 弱钝化 | 邻/对位 | |
| −I | 弱钝化 | 邻/对位 | |
| 间位定位基 (钝化) | −NO2 | 强钝化 | 间位 |
| −CF3, −CCl3 | 强钝化 | 间位 | |
| −CN, −SO3H | 强钝化 | 间位 | |
| −CHO, −COR, −COOH, −COOR | 中等钝化 | 间位 | |
| −CONH2, −NR3+ | 中等~强钝化 | 间位 |
| 条件 | 反应类型 | 位置 | 示例 |
|---|---|---|---|
| Lewis酸(FeBr3) | 亲电取代 | 苯环上 | 甲苯+Br2/FeBr3→邻/对溴甲苯 |
| hv / NBS / 高温 | 自由基取代 | 侧链α-H | 甲苯+Br2/hv→苄基溴(C6H5CH2Br) |
| KMnO4 | 氧化 | 侧链→COOH | 甲苯→苯甲酸 |
苯 + O2,V2O5催化,500°C → 顺丁烯二酸酐(马来酸酐)
苯 → 1,4-环己二烯(部分还原,保留两个非共轭双键)
供电子基(EDG)取代苯(如 -OCH3, -CH3):
产物:取代基连在双键碳上(2,5-二氢产物)
例:苯甲醚(C6H5OCH3) → 1-甲氧基-1,4-环己二烯(2,5-二氢苯甲醚)
OCH₃ OCH₃
| |
/===\ Na/NH₃ /==\
|| || ------→ | |
\===/ EtOH \==/
1,4-二烯(C1=C2, C5=C6未被还原)
解释:EDG增加苯环电子密度 → 电子不易被加上 → 还原发生在EDG远端(C3,C6位被还原加H)→ EDG所在碳保留在双键上。
吸电子基(EWG)取代苯(如 -COOH, -COOR, -COR):
产物:取代基连在非双键碳(sp3碳)上(1,4-二氢产物)
例:苯甲酸(C6H5COOH) → 1-羧基-2,5-环己二烯-1-羧酸 → 2,5-环己二烯-1-羧酸(1,4-二氢苯甲酸)
COOH COOH
| |
/===\ Na/NH₃ H-C-H
|| || ------→ /==\
\===/ EtOH || ||
\==/
1,4-二烯(C2=C3, C5=C6未被还原)
解释:EWG降低苯环电子密度 → 电子易加到EWG所在碳 → 还原发生在EWG近端(C1位被还原加H)→ EWG所在碳变为sp3,双键移到C2=C3和C5=C6位。
| 名称 | 环数 | π电子数 | 特点 |
|---|---|---|---|
| 萘 | 2 | 10 | 芳香性比苯弱,反应活性更高 |
| 蒽 | 3(线形) | 14 | 9,10-位最活泼 |
| 菲 | 3(角形) | 14 | 9,10-位最活泼 |
• 稠环芳烃的芳香性:萘 > 蒽/菲;环数越多,越容易加成
• 蒽的9,10-位可发生Diels-Alder反应(作为双烯体)
(a) 环戊二烯负离子 (C5H5−)
分析:5个碳原子均为sp2杂化,各贡献1个p轨道参与共轭。5个碳上分配的π电子:4个碳各贡献1个电子(来自双键),带负电荷的碳贡献2个电子(孤对电子进入p轨道)。
π电子总数 = 6个(4n+2, n=1)
环状共轭 ✓ | 共平面 ✓ | 4n+2 ✓ → 芳香性
这解释了环戊二烯的酸性(pKa≈16)远强于一般烃——失去H+后生成芳香性稳定阴离子。
(b) 环戊二烯正离子 (C5H5+)
分析:5个碳sp2杂化,正电荷碳的p轨道为空。
π电子总数 = 4个(4n, n=1)
环状共轭 ✓ | 共平面 ✓ | 4n → 反芳香性,极不稳定
这就是为什么环戊二烯极难失去H−形成正离子——产物反芳香,能量极高。
(c) 环丙烯正离子 (C3H3+)
分析:3个碳sp2杂化,正电荷碳p轨道空。2个碳各贡献1个π电子。
π电子总数 = 2个(4n+2, n=0)
环状共轭 ✓ | 共平面 ✓ | 4n+2 ✓ → 芳香性
这是最小的芳香体系!环丙烯正离子盐(如C3H3+Cl−)确实能被制备并稳定存在。
(d) 环辛四烯 (C8H8, COT)
分析:8个π电子,4n(n=2)。若平面共轭将为反芳香(极不稳定),因此分子采取船式(tub-shaped)非平面构象,交替单双键,p轨道不连续重叠。
非平面 → 不满足Hückel规则前提 → 非芳香性(既非芳香也非反芳香)
COT的化学性质类似普通多烯:能使Br2/CCl4褪色,可加氢。有趣的是,COT2−(接受2个电子后变为10π,且变平面)具有芳香性。
(e) 吡咯
分析:吡咯是五元含氮杂环。4个碳和1个氮均sp2杂化,N的孤对电子进入p轨道参与共轭(N不是用孤对做碱,而是贡献给芳香体系)。
4个C各贡献1个π电子 + N贡献2个π电子 = 6个π电子(4n+2, n=1)
环状共轭 ✓ | 共平面 ✓ | 4n+2 ✓ → 芳香性
这解释了吡咯的碱性极弱(pKb≈13.6)——N的孤对电子参与芳香π体系,不能再接受质子(接受H+将破坏芳香性)。与之对比,吡啶的N孤对电子在sp2轨道中(不参与π体系),碱性正常。
(a) 甲苯 + HNO3/H2SO4
(b) 硝基苯 + Br2/FeBr3
(c) 苯甲醚 + CH3COCl/AlCl3
(d) 苯酚 + Br2/H2O(过量)
(e) 萘 + Br2/FeBr3(低温)
(f) 萘 + SO3/H2SO4(160°C)
(a) 甲苯 + HNO3/H2SO4 → 邻硝基甲苯 + 对硝基甲苯
-CH3为弱活化邻对位定位基(超共轭供电子),NO2+进入邻位和对位。邻:对比例约58:37(对位因位阻较小略少于统计预测的2:1)。反应速率比苯快约25倍。
(b) 硝基苯 + Br2/FeBr3 → 间溴硝基苯
-NO2为强钝化间位定位基(强-I和-C效应使邻对位电子密度大幅降低)。Br+进入间位(实际是间位被钝化最少)。反应速率比苯慢约106倍,需要较强条件。
(c) 苯甲醚(C6H5OCH3) + CH3COCl/AlCl3 → 对甲氧基苯乙酮
-OCH3为强活化邻对位定位基(O的孤对电子通过+C效应向环供电子)。酰基正离子CH3CO+进入对位为主(邻位有-OCH3的位阻)。F-C酰基化不重排、只得一元取代产物。
(d) 苯酚 + Br2/H2O(过量) → 2,4,6-三溴苯酚(白色沉淀)
-OH为极强活化邻对位定位基。苯酚活性极高,无需Lewis酸催化,在水溶液中Br2即可直接反应。由于活性太强,三个邻对位全部被溴代。这是鉴别苯酚的经典反应。
注意:若要得到一元溴代产物,需要降低活性:在CS2低温中用恰好1当量Br2,得对溴苯酚为主。
(e) 萘 + Br2/FeBr3(低温) → 1-溴萘(α-溴萘)
低温属于动力学控制。α位取代的σ络合物中间体更稳定(正电荷有更多共振结构分散,不破坏完整苯环的共振结构有2个 vs β位的1个)。因此α位取代活化能低,动力学有利。
(f) 萘 + SO3/H2SO4(160°C) → β-萘磺酸(2-萘磺酸)
高温属于热力学控制。磺化是可逆反应!在160°C高温下,α-萘磺酸可以脱磺酸后重新磺化。β位产物位阻更小、热力学更稳定(peri位无H-H排斥)。长时间高温达到热力学平衡后,β-产物占优。
活性排序(由高到低):
苯酚(-OH) > 苯甲醚(-OCH3) > 甲苯(-CH3) > 苯(-H) > 氯苯(-Cl) > 硝基苯(-NO2)
分析:
定位效应:苯酚、苯甲醚、甲苯 → 邻对位定位(活化);氯苯 → 邻对位定位(钝化);硝基苯 → 间位定位(钝化)
4-甲基苯甲酸结构:1位-COOH,4位-CH3
定位分析:
两个基团定位一致:都指向3位和5位!(协同定位)
结论:新的-NO2进入2位(即-COOH的邻位=-CH3的间位)。
等等——重新分析:-CH3在4位,其邻位=3,5位;-COOH在1位,其间位=3,5位。两者一致指向3位(或等价的5位)。
但还要考虑位阻:3位紧邻1位的-COOH,不利;5位空间更开阔。
最终答案:主要产物为2-硝基-4-甲基苯甲酸(NO2进入2位)——因为-CH3活化能力 > -COOH钝化能力,-CH3的邻位(3位)和对位(1位已占)中,实际上最可能位置是-CH3的邻位=3位,也就是-COOH的间位,产物为3-硝基-4-甲基苯甲酸。由于分子的对称性,3位=5位等价时不等价(3位邻近COOH),实际主产物为在2位硝化(-CH3的间位,但也是-COOH的邻位)。
正确分析:当两个定位基矛盾时(-CH3活化 vs -COOH钝化),以活化能力强的-CH3为主。-CH3在4位,其邻位=3,5位。同时3位也是-COOH的间位(一致!)。主产物:3-硝基-4-甲基苯甲酸。一般不进入两个基团之间的拥挤位置(2位)。
目标:Br在对位,NO2在1位(即对位关系)。
正确路线(先硝化再溴代——错误!先溴代再硝化——也要分析):
分析两种顺序:
方案A:先硝化 → 硝基苯 + Br2/FeBr3 → 间溴硝基苯(-NO2间位定位)❌ 得到间位,不是对位!
方案B:先溴代 → 溴苯 + HNO3/H2SO4 → 邻硝基溴苯 + 对硝基溴苯(-Br邻对位定位)✓ 取对位产物即可!
正确路线:
① 苯 + Br2/FeBr3 → 溴苯
② 溴苯 + HNO3/H2SO4 → 对溴硝基苯(-Br为邻对位定位,取对位主产物)
为什么顺序重要:-Br是邻对位定位基,能把-NO2引到对位。若先引入-NO2(间位定位基),Br只能进间位,永远得不到对位产物。
分析:-C2H5是邻对位定位基,-Cl也是邻对位定位基。两个邻对位定位基不可能通过简单连续取代得到间位产物!需要间接方法。
策略:利用-COCH3(间位定位基)先定位,再还原为-C2H5
① 苯 + CH3COCl/AlCl3 → 苯乙酮(F-C酰基化)
② 苯乙酮 + Cl2/FeCl3 → 间氯苯乙酮(-COCH3为间位定位基,Cl进间位)
③ 间氯苯乙酮 + Zn-Hg/HCl(Clemmensen还原) → 间氯乙基苯
为什么不能直接做:
• 先引入-C2H5再氯代 → -C2H5是邻对位定位 → 得到邻/对氯乙基苯 ❌
• 先氯代再引入-C2H5 → -Cl也是邻对位定位 → F-C烷基化进入邻对位 ❌
• 唯一方法:利用酰基(间位定位基)先定位Cl到间位,然后还原酰基为烷基。
两个间位定位基处于对位关系——不能通过先引入一个间位定位基再定位另一个得到对位产物。需要利用-CH3的邻对位定位。
正确路线:
① 甲苯 + HNO3/H2SO4 → 对硝基甲苯(-CH3邻对位定位,取对位产物)
② 对硝基甲苯 + KMnO4/H+,Δ → 对硝基苯甲酸(氧化侧链-CH3→-COOH)
为什么不能反过来:
若先氧化甲苯为苯甲酸(-COOH间位定位),再硝化 → NO2进入间位 → 得到间硝基苯甲酸 ❌
核心原则:-CH3先当"邻对位定位代理人",引导-NO2到对位后,再氧化为-COOH。顺序决定成败!
直接三次溴代苯不可行:第一个Br是邻对位定位,第二个Br进入第一个的邻/对位,最终得到1,2,4-三溴苯而非1,3,5。
策略:利用苯胺的强活化性 + 重氮化脱氨
① 苯 + HNO3/H2SO4 → 硝基苯
② 硝基苯 + Fe/HCl → 苯胺(还原-NO2为-NH2)
③ 苯胺 + 3Br2/H2O → 2,4,6-三溴苯胺(-NH2极强活化,邻对位全部溴代,无需催化剂)
④ 2,4,6-三溴苯胺 + NaNO2/H2SO4, 0°C → 重氮盐
⑤ 重氮盐 + H3PO2(次磷酸)→ 1,3,5-三溴苯 + N2↑
为什么这样设计:
• -NH2作为"超强活化+导向基",一次性把三个邻对位全部溴代(得到1,3,5-三溴相对于NH2)
• 重氮化-脱氮反应(用H3PO2还原)去除-NH2,只留下三个Br
• 这是"导向基安装-使用-拆除"的经典策略
路线一(经对硝基甲苯)——最经典方法:
① 苯 + CH3Cl/AlCl3 → 甲苯
② 甲苯 + HNO3/H2SO4 → 对硝基甲苯(-CH3邻对位定位,取对位)
③ 对硝基甲苯 + KMnO4/H+,Δ → 对硝基苯甲酸(氧化侧链)
④ 对硝基苯甲酸 + Fe/HCl(或H2/Pd) → 对氨基苯甲酸(还原-NO2为-NH2)
逻辑:用-CH3的邻对位定位引入-NO2 → 氧化-CH3 → 还原-NO2
路线二(经对溴甲苯→Grignard):
① 苯 + CH3Cl/AlCl3 → 甲苯
② 甲苯 + HNO3/H2SO4 → 对硝基甲苯
③ 对硝基甲苯 + KMnO4 → 对硝基苯甲酸
④ 还原 → 对氨基苯甲酸
(路线二本质相同,展示了这是最优策略)
为什么不能直接从苯胺出发?
苯胺(-NH2是强活化邻对位定位基) + 引入-COOH?F-C酰基化不能用于胺(-NH2与AlCl3配位使催化剂失活)。即使能反应,也只能到邻/对位,而非间位。所以必须走间接路线。
(a) 甲苯 + Cl2/hv → C6H5CH2Cl(苄基氯/氯化苄)
机理:自由基链式反应
• 引发:Cl2 →(hv)→ 2Cl·
• 传递:C6H5CH3 + Cl· → C6H5CH2·(苄基自由基) + HCl
• C6H5CH2· + Cl2 → C6H5CH2Cl + Cl·
苄基自由基因与苯环共轭而特别稳定,所以侧链α-H优先被取代。
(b) 甲苯 + Cl2/FeCl3 → 邻氯甲苯 + 对氯甲苯
机理:亲电芳香取代
FeCl3活化Cl2产生Cl+亲电试剂 → 进攻苯环π电子 → σ络合物 → 失去H+恢复芳香性。
-CH3为邻对位定位基,Cl进入邻位和对位。
总结:同一底物(甲苯)+ 同一试剂(Cl2),仅催化条件不同,产物完全不同!这是考试必考的辨析点。
产物:苯甲酸 C6H5COOH(不是苯乙酸C6H5CH2COOH!)
规律:KMnO4氧化芳烃侧链时,无论侧链有多长,都从α碳断裂,最终侧链变为-COOH。
前提:侧链必须有α-H(苄位氢),氧化从Cα-H键的均裂开始。无α-H的叔丁基苯完全不被氧化。
苯甲醚(供电子基-OCH3)的Birch还原:
Na/液NH3/EtOH → 2,5-二氢苯甲醚(1-甲氧基-1,4-环己二烯)
-OCH3所在碳保留在双键上(sp2不变)。还原发生在远端的C3和C6位。
解释:供电子基增加苯环电子密度 → 电子不易被加上 → 还原发生在EDG远端 → EDG碳保持sp2。
苯甲酸(吸电子基-COOH)的Birch还原:
Na/液NH3/EtOH → 2,5-环己二烯-1-羧酸(1,4-二氢苯甲酸)
-COOH所在碳变为sp3(失去双键),双键移到C2=C3和C5=C6位。
解释:吸电子基降低苯环电子密度 → 电子容易加到EWG所在碳 → 还原发生在EWG近端 → EWG碳变为sp3。
记忆口诀:供电子"留双键"(取代基碳上有双键),吸电子"去双键"(取代基碳上双键被还原掉)。两种产物都是1,4-环己二烯型(非共轭二烯)。
第一步:分析分子式
C9H12,不饱和度 = (2×9+2-12)/2 = 4,恰好等于苯环(3双键+1环=4),说明只有苯环无其他不饱和结构。
第二步:分析氧化产物
KMnO4氧化只得到一种产物:苯甲酸(C6H5COOH)——即只有一个-COOH。
这意味着苯环上只有一条侧链被氧化为-COOH。
第三步:确定侧链
C9H12 - C6H5(苯环) = C3H7(一条丙基侧链)
只有一种氧化产物 → 只有一条侧链 → A为丙基苯
但丙基可以是正丙基或异丙基:
两者都只给一种产物(苯甲酸),仅靠此条件无法区分。但若题目强调"只得到一种产物"是排除其他C9H12异构体的条件:
但这些产物都不是苯甲酸!所以A必须是正丙基苯或异丙基苯(均给苯甲酸一种产物)。
第一步:列出C8H10的异构体
不饱和度 = (2×8+2-10)/2 = 4 → 苯环。C8H10 - C6H4 = C2H6(两个甲基或一个乙基)
第二步:分析每种异构体硝化产物数目
对二甲苯:分子对称性最高。两个-CH3协同定位,硝化只能进入2位(=3位等价)→ 1种产物 → A = 对二甲苯
邻二甲苯:-CH3在1,2位。硝化可进入3位或4位(两者不等价) → 2种产物
乙苯:-C2H5在1位。硝化进入邻位(2位)或对位(4位)(注意2位和6位因乙基不对称而不等价?不对,乙苯中2位=6位等价,所以邻位和对位 → 2种产物)
间二甲苯:-CH3在1,3位。硝化可进入2位、4位、5位(4位=6位等价?不对——4位≠5位) → 实际可能位置:2位(两个CH3之间)、4位(=6位)、5位 → 3种产物
最终答案:
A(1种产物) = 对二甲苯
B(2种产物) = 邻二甲苯(或乙苯)
C(2种产物) = 乙苯(或邻二甲苯)
D(3种产物) = 间二甲苯