第6章 炔烃和二烯烃
核心知识点
6.1 炔烃的结构
sp杂化:碳碳三键由 1个σ键 + 2个π键组成,两个sp杂化碳原子呈直线形(键角180°)。
键参数对比
| 杂化 | 键长(C-C) | 键能 | s成分 | 电负性 |
|---|
| sp (C≡C) | 0.120 nm | 837 kJ/mol | 50% | 最大 |
| sp2 (C=C) | 0.134 nm | 611 kJ/mol | 33% | 中等 |
| sp3 (C-C) | 0.154 nm | 347 kJ/mol | 25% | 最小 |
s成分越大 → 电子越靠近原子核 → 电负性越大 → C-H键极性越强 → 酸性越强
炔烃的物理性质
- 沸点:略高于同碳数的烷烃和烯烃。原因:炔烃分子呈细长线形,分子间接触面积大,范德华力(色散力)较强。
- 密度:均小于1(比水轻)。
- 溶解性:难溶于水,易溶于苯、CCl4、乙醚等有机溶剂。
6.2 端炔的酸性
pKa比较
| 化合物 | 杂化 | pKa |
|---|
| RC≡CH(端炔) | sp | ≈ 25 |
| R2C=CH2(烯烃) | sp2 | ≈ 44 |
| R3CH(烷烃) | sp3 | ≈ 50 |
| H2O | — | 15.7 |
| NH3 | — | 38 |
只有端炔有酸性!内炔(如2-丁炔 CH3C≡CCH3)没有sp杂化C-H键,不能形成炔钠。
炔钠的合成应用(增碳链)
RC≡C−Na+ + R'CH2X → RC≡C-CH2R'(SN2反应)
例:HC≡CH ⟶NaNH₂; HC≡C−Na+ ⟶CH₃CH₂Br; HC≡C-CH2CH3(1-丁炔)
6.3 炔烃的加成反应
一、加卤素(Br2、Cl2)
• 1 mol Br2 → 反式二溴烯烃(反式加成)
• 过量 Br2 → 四溴烷烃(完全加成)
RC≡CR' + Br2 → 反式-RCBr=CR'Br ⟶Br₂; RCBr2-CR'Br2
二、加HX(马氏规则)
• 1 mol HX → 卤代烯烃(马氏,X加在含H较少的C上)
• 过量 HX → 偕二卤代烷(两个X在同一碳上)
三、水合反应(Kucherov反应)——重要!
条件:HgSO4 / H2SO4 / H2O
烯醇-酮互变异构:烯醇式不稳定,自发转变为酮式。这是重要的有机化学概念。
四、硼氢化-氧化(反马氏水合)
端炔 + R2BH → 烯基硼烷 ⟶H₂O₂/NaOH; 醛(反马氏,OH加到端碳)
对比记忆:Kucherov水合(马氏)→ 酮;硼氢化-氧化(反马氏)→ 醛。互补方法!
五、硼氢化-还原(制备顺式烯烃)
炔烃经硼氢化后,用CH3COOH(而非H2O2/NaOH)处理烯基硼烷,可得到顺式烯烃。
RC≡CR' ⟶R₂BH; 烯基硼烷 ⟶CH₃COOH; (Z)-RCH=CHR'(顺式烯烃)
对比:硼氢化-氧化(H2O2/NaOH)→ 醛;硼氢化-还原(CH3COOH)→ 顺式烯烃。两条不同的后处理路线!
六、过氧化物效应(反马氏HBr加成)
炔烃 + HBr + 过氧化物(ROOR) → 反马氏产物(自由基加成机理)
RC≡CH + HBr ⟶ROOR; RCH=CHBr(Br加在端碳上,反马氏)
注意:过氧化物效应只对HBr有效,对HCl和HI无效!机理为自由基链式反应。
七、炔烃的亲核加成反应
炔烃能发生亲核加成,而烯烃不能。原因:三键的π电子云密度大,且sp碳电负性大,有利于亲核试剂进攻。反应需碱催化或高温高压条件。
| 反应物 | 条件 | 产物 | 应用 |
|---|
| HC≡CH + CH3OH | KOH催化,160-165°C | CH2=CH-OCH3(甲基乙烯基醚) | 有机合成中间体 |
| HC≡CH + CH3COOH | 催化剂 | CH2=CH-OOCCH3(醋酸乙烯酯) | 乳胶漆、粘合剂原料 |
| HC≡CH + HCN | 催化剂 | CH2=CH-CN(丙烯腈) | 合成腈纶纤维 |
"乙烯基化反应":上述反应的共同特征是将 CH2=CH- 基团(乙烯基)引入其他分子中,因此统称为乙烯基化反应。这是乙炔工业应用的重要途径。
炔烃亲电加成比烯烃慢的原因
虽然炔烃有更多的π电子,但其亲电加成反应速率反而比烯烃慢,原因有二:
- Csp电负性 > Csp²:sp杂化碳s成分大(50%),对π电子束缚更紧,不易提供给亲电试剂
- 中间体稳定性:炔烃亲电加成的中间体为烯基碳正离子(C+为sp杂化),不如烯烃加成的烷基碳正离子(C+为sp2杂化)稳定
6.4 炔烃的还原(立体选择性)——必考!
| 还原条件 | 产物 | 立体化学 | 机理 |
|---|
| H2 / Lindlar催化剂 | Z-烯烃(顺式) | 顺式加氢 | 催化表面同侧加H |
| Na / 液NH3 | E-烯烃(反式) | 反式还原 | 自由基阴离子中间体 |
| H2(过量) / Pt或Pd | 烷烃 | 完全加氢 | 两步加氢 |
口诀:Lindlar → 顺(Z),Na/NH₃ → 反(E)。这两种方法互补,可选择性地制备Z或E烯烃。
第4题考点:制备(Z)-2,3-二氘代丁-2-烯
• D2/Lindlar → 顺式加氘 → (Z)构型 ✓
• Na/液ND3 → 反式加氘 → (E)构型 ✗
判断关键:看加成方式是顺式还是反式!
6.5 端炔的鉴别反应
银镜/铜镜反应(定性鉴别端炔)
| 试剂 | 反应 | 现象 |
|---|
| Ag(NH3)2+(银氨溶液) | RC≡CH → RC≡CAg↓ | 白色沉淀(炔化银) |
| Cu(NH3)2+(铜氨溶液) | RC≡CH → RC≡CCu↓ | 红棕色沉淀(炔化亚铜) |
注意:只有端炔(含C≡C-H)能反应!内炔不能。
炔化银干燥后受热易爆炸,实验后需用稀HNO3分解。
化学鉴别思路:Br2/CCl4 区分饱和/不饱和 → Ag(NH3)2+ 区分端炔/烯烃/内炔
6.6 炔烃的氧化
KMnO4氧化(强氧化)
• 端炔 + KMnO4(酸性/热) → RCOOH + CO2
• 内炔 + KMnO4(酸性/热) → 两个羧酸
例:CH3C≡CCH3 ⟶KMnO₄/H⁺; 2 CH3COOH
例:CH3CH2CH(CH3)CH2CH=CHCH3(含双键) ⟶KMnO₄/H⁺; 相应羧酸
氧化反应可用于推断炔烃结构:通过分析氧化产物(羧酸),可以反推三键的位置。
6.7 共轭二烯烃
二烯烃分类
| 类型 | 结构特征 | 例子 | 稳定性 |
|---|
| 累积二烯 | C=C=C(相邻) | 丙二烯 CH2=C=CH2 | 不稳定 |
| 共轭二烯 | C=C-C=C(交替) | 1,3-丁二烯 | 最稳定(离域能) |
| 孤立二烯 | C=C-(CH2)n-C=C | 1,4-戊二烯 | 中等 |
共轭稳定化
• 1,3-丁二烯的氢化热 = 237 kJ/mol,而两个孤立双键预期 = 2×127 = 254 kJ/mol
• 离域能(共轭能) = 254 - 237 = 17 kJ/mol,说明共轭体系更稳定
s-cis 与 s-trans 构象
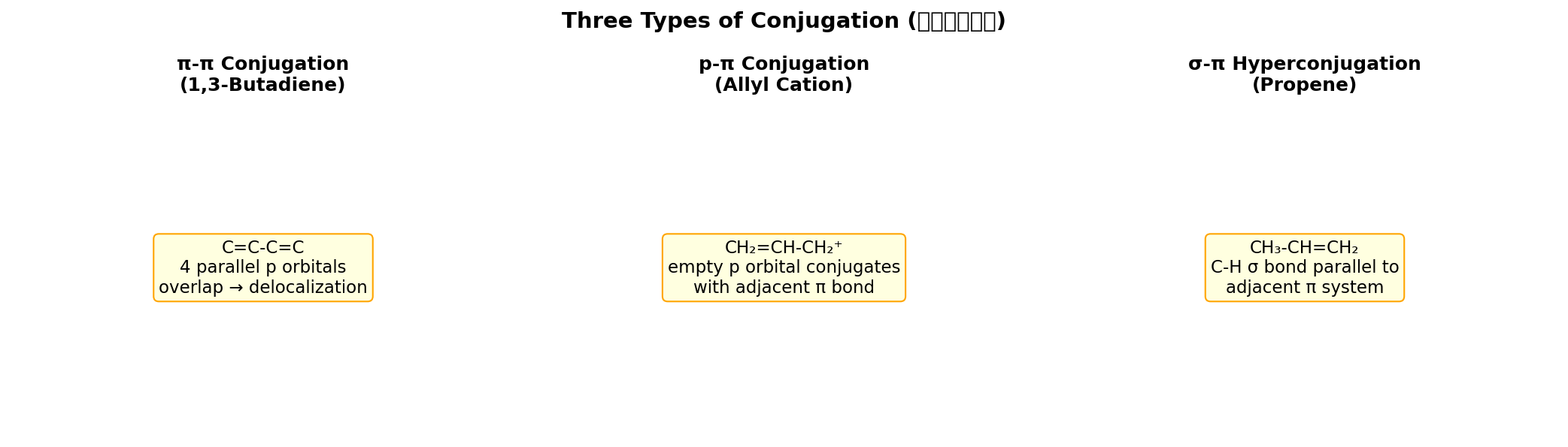
超共轭效应:σ键(通常C-H键)与相邻π键或空轨道相互作用,导致电子离域化,可解释烷基正离子稳定性。
共轭体系分类
| 类型 | 特征 | 典型例子 |
|---|
| π-π共轭 | 单键两侧各有一个π键,π电子通过p轨道连续重叠而离域 | 1,3-丁二烯 CH2=CH-CH=CH2 |
| p-π共轭 | 单键一侧为π键,另一侧原子提供p轨道(含孤对电子或空轨道)参与共轭 | 烯丙基碳正离子 CH2=CH-CH2+(空p轨道);氯乙烯中Cl的p轨道与C=C共轭 |
| σ-π超共轭 | C-H的σ键与相邻碳上的π键(或空p轨道)发生部分重叠 | 丙烯中甲基C-H与C=C的超共轭;碳正离子稳定性解释 |
共轭效果:π-π共轭 > p-π共轭 > σ-π超共轭。共轭使体系能量降低、键长趋于平均化。
重要定义
- 氢化热:1 mol不饱和化合物经催化加氢时所放出的热量。氢化热越小,说明分子越稳定。可用于比较异构体、共轭与非共轭体系的相对稳定性。
- 离域能(共轭能):共轭体系的实际能量与假设各双键孤立(无共轭)时的能量之差。例如1,3-丁二烯的离域能 = 2×127 - 237 = 17 kJ/mol,表明共轭稳定化的程度。
6.8 1,2-加成 vs 1,4-加成(动力学 vs 热力学控制)
为什么1,4-加成产物更稳定?
1,4-加成产物为内烯烃(双键在链内),有更多的σ-π*超共轭作用,分子更稳定。
1,2-加成产物为端烯烃(双键在链端),超共轭少,稳定性较低。
烯丙基碳正离子
共轭二烯加HX的第一步:H+加到C1,生成烯丙基碳正离子(p轨道与双键共轭,正电荷离域在C2和C4上)
• Br−进攻C2 → 1,2-加成产物
• Br−进攻C4 → 1,4-加成产物
6.9 Diels-Alder反应 [4+2]环加成——必考!
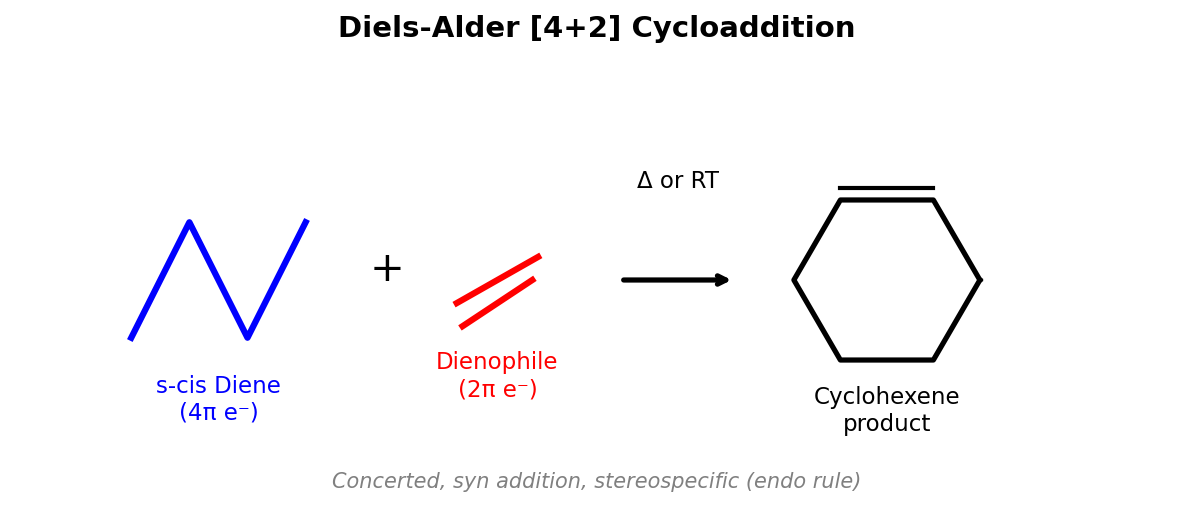
D-A反应三大要点
- s-cis构象:二烯必须采取s-cis构象才能反应(环戊二烯被"锁"在s-cis,反应活性极高)
- 电子匹配:二烯(富电子)+ 亲双烯体(缺电子,含-CHO、-COOH、-CN、-NO2等吸电子基)
- endo规则:endo产物为动力学主产物(取代基朝向二烯方向)
经典D-A反应实例
| 二烯 | 亲双烯体 | 产物 |
|---|
| 1,3-丁二烯 | 顺丁烯二酸酐 | 四氢邻苯二甲酸酐 |
| 1,3-丁二烯 | 丙烯醛 CH2=CHCHO | 环己烯-4-甲醛 |
| 环戊二烯 | 顺丁烯二酸酐 | 降冰片烯二酸酐 |
| 1,3-丁二烯 | DEAD(丁炔二酸二乙酯) | 环己二烯二酸二乙酯 |
逆D-A反应(反推原料)
在六元环产物中找到双键,从双键两侧"切开",还原回二烯和亲双烯体。
氯丁二烯聚合:CH2=C(Cl)-CH=CH2 可发生1,4-加聚反应,生成氯丁橡胶。
课后习题精选
题1 炔烃反应
题1 完成下列炔烃反应,写出主要产物:
(a) 1-丁炔 + 1当量HBr
(b) 1-丁炔 + 2当量HBr
(c) 1-丁炔 + H2O/H2SO4/HgSO4
(d) 2-丁炔 + H2/Lindlar催化剂
(e) 2-丁炔 + Na/NH3(l)
(f) 1-丁炔 + NaNH2 → 然后+CH3I
(g) 丙炔 + 2当量Br2
(h) 1-丁炔 + BH3·THF → H2O2/NaOH(硼氢化)
解题思路:炔烃比烯烃多一个π键,可发生两次亲电加成。末端炔有酸性C-H(pKa≈25),可用强碱脱质子→炔负离子→亲核试剂。
| 反应 | 产物 | 要点 |
|---|
| (a) +1eq HBr | 2-溴-1-丁烯 CH3CH2CBr=CH2 | Markovnikov:H加到末端C,Br加到内部C→乙烯基溴 |
| (b) +2eq HBr | 2,2-二溴丁烷 CH3CH2CBr2CH3 | 两次Mark→同碳二卤(geminal) |
| (c) +H2O/Hg2+ | 2-丁酮 CH3COCH2CH3 | Mark水合→烯醇→互变异构为酮(末端炔→甲基酮) |
| (d) H2/Lindlar | cis-2-丁烯 | Lindlar=毒化Pd,只加一当量H2,syn→cis烯烃 |
| (e) Na/NH3 | trans-2-丁烯 | 溶剂金属还原→反式烯烃(自由基阴离子机理) |
| (f) NaNH2→CH3I | 2-戊炔 CH3C≡CCH2CH3 | 炔负离子SN2烷基化(只能用1°卤代烃!) |
| (g) +2eq Br2 | 1,1,2,2-四溴丙烷 | 两次anti加成 |
| (h) 硼氢化 | 丁醛 CH3CH2CH2CHO | anti-Mark水合→烯醇→醛(末端炔硼氢化→醛,区别于Hg2+→酮) |
必记对比:末端炔水合→Hg2+催化给甲基酮(Mark);硼氢化给醛(anti-Mark)。这是合成设计中选择性控制的核心。
立体选择性对比:Lindlar加氢→cis烯;Na/NH3→trans烯。两种方法从同一炔烃得到几何异构体!
题2 Diels-Alder反应
题2 
预测下列DA反应的产物(注意立体化学和区域选择性):
(a) 1,3-丁二烯 + 丙烯醛(CH
2=CHCHO)
(b) 2,3-二甲基-1,3-丁二烯 + 马来酸酐
(c) 环戊二烯 + 丙烯酸甲酯(endo/exo)
(d) 1-甲氧基-1,3-丁二烯 + 丙烯腈(区域选择性)
解题思路:DA反应=协同[4+2]环加成。必须条件:①二烯s-cis构象 ②电子互补(富电子二烯+缺电子亲二烯体) ③syn加成(endo规则)。
(a) 丁二烯 + 丙烯醛:
产物:4-甲酰基环己烯(环己烯-4-甲醛)。新环6员,双键在C1-C2位(原二烯中间两碳形成的σ键旁边)。CHO在C4位。
(b) 2,3-二甲基丁二烯 + 马来酸酐:
产物:4,5-二甲基-4-环己烯-1,2-二甲酸酐。两个甲基在双键上(原二烯C2,C3→产物C4,C5上双键)。马来酸酐的两个C=O保持cis关系。
立体:马来酸酐中两个酸酐C=O本身cis→产物中也是cis(syn加成保持)。
(c) 环戊二烯 + 丙烯酸甲酯:
环戊二烯固定为s-cis(环状锁定)。产物:双环[2.2.1]庚-5-烯-2-甲酸甲酯(降冰片烯衍生物)。
endo规则:亲二烯体的C=O基团朝向环内(endo方向)→动力学产物。
endo产物为主(次级轨道相互作用稳定过渡态)。exo产物为热力学产物(更稳定但动力学不利)。
(d) 1-甲氧基丁二烯 + 丙烯腈(区域选择性):
1-甲氧基=给电子(EDG在二烯C1),CN=吸电子(EWG在亲二烯体)。
"ortho"规则:EDG和EWG在产物中为1,2-关系(邻位)。
产物:2-甲氧基-4-氰基环己烯(OCH3在C1旁=C2,CN在C4=对应亲二烯体碳)。
DA区域选择性规律:给电子基(二烯)与吸电子基(亲二烯体)倾向于"ortho"或"para"关系→由前线轨道系数大小决定。
题3 1,2-加成与1,4-加成
题3
(a) 1,3-丁二烯 + 1当量HBr → 写出1,2-和1,4-加成产物,解释温度对比例的影响。
(b) 2-甲基-1,3-丁二烯(异戊二烯) + 1当量HCl → 所有可能产物及比例分析。
解题思路:共轭二烯加成第一步形成烯丙型碳正离子→C2或C4(1,4位)都有正电荷→亲核试剂攻击两个位点。低温=动力学控制(1,2);高温=热力学控制(1,4)。
(a) 1,3-丁二烯 + HBr:
步骤1:H+加到C1(末端,形成更稳定的烯丙基碳正离子):
CH3-+CH-CH=CH2 ↔ CH3-CH=CH-CH2+
步骤2:Br−进攻→
| 产物 | 类型 | 结构 |
|---|
| 3-溴-1-丁烯 | 1,2-加成 | CH3CHBrCH=CH2 |
| 1-溴-2-丁烯(E/Z) | 1,4-加成 | CH3CH=CHCH2Br |
温度效应:−80°C→1,2产物为主(80%)(动力学控制:Br−攻击离它更近的C2更快)。
40°C→1,4产物为主(80%)(热力学控制:内部烯烃更稳定)。
(b) 异戊二烯 + HCl:CH2=C(CH3)-CH=CH2
H+加到C1(形成C2上3°烯丙型正离子,最稳定):
CH3-+C(CH3)-CH=CH2 ↔ CH3-C(CH3)=CH-CH2+
1,2-加成→3-氯-2-甲基-1-丁烯:CH2=C(CH3)CHClCH3...不对。
修正:H加到C1→C2正电荷(3°!): (CH3)(Cl)C=... Cl−攻C2→3-氯-2-甲基-1-丁烯(1,2)。
Cl−攻C4→1-氯-2-甲基-2-丁烯(1,4)。
1,4-产物更取代(三取代烯)→热力学更稳定→高温主要产物。
1,4-加成产物往往是更取代的内部烯烃→热力学更稳定。所以高温有利于1,4-加成(热力学控制)。
题4 鉴别
题4 用化学方法鉴别:1,3-环己二烯、环己烯、苯。
三者都含不饱和度,关键区别:苯具有芳香性(不易加成)。
| 试剂 | 1,3-环己二烯 | 环己烯 | 苯 |
|---|
| Br2/CCl4 | 褪色(快,加2eq) | 褪色(加1eq) | 不褪色 |
| KMnO4(冷稀) | 褪色 | 褪色 | 不褪色 |
| Br2计量 | 消耗2当量 | 消耗1当量 | 0 |
方案:①Br2/CCl4不褪色→苯。②测Br2消耗量:2当量→1,3-环己二烯,1当量→环己烯。
或用DA反应:1,3-环己二烯可作二烯参与DA反应(如与马来酸酐加热)→环己烯不能。
题5 推断
题5
(a) 化合物A(C5H8)与2当量H2/Pd→正戊烷。A的臭氧分解→甲醛+丙醛(两种产物)。推断A结构。
(b) 化合物B(C6H10)与1当量H2/Lindlar催化剂→C6H12(仍有1个不饱和度)。B+过量H2→环己烷。推断B结构。
(a) C5H8,DBE=(10+2-8)/2=2。加2当量H2→正戊烷(无环)→2个双键或1个三键。
臭氧分解→甲醛(HCHO)+丙醛(CH3CH2CHO)。如果是二烯切断两个C=C:
CH2=CH-CH=CH-CH3? 切断→HCHO + OHC-CHO + CH3CHO? 不对,会有乙二醛。
如果是二烯CH2=CH-CH2-CH=CH2(1,4-戊二烯)→臭氧分解:切C1=C2→HCHO + OHC-CH2-CH=CH2,再切→HCHO + OHC-CH2-CHO。得到2×HCHO + 丙二醛。不符。
若A为1,3-戊二烯CH3CH=CH-CH=CH2:臭氧切每个C=C→CH3CHO + OHC-CHO + HCHO。得到甲醛+丙醛+乙二醛...还是不符。
若A含三键:1-戊炔 CH≡C-CH2CH2CH3,加2eq H2→正戊烷✓。臭氧分解炔:HC≡C切断→HCHO?(不对,炔臭氧分解→羧酸)。
重新考虑:A = 1,4-戊二烯 CH2=CHCH2CH=CH2→臭氧分解:HCHO + OHCCH2CHO + HCHO=甲醛+丙二醛。不是丙醛。
答:A = 1,3-戊二烯(CH2=CH−CH=CHCH3)。臭氧分解共轭二烯→HCHO + 乙二醛 + CH3CHO。题目简化为"甲醛+丙醛"可能是指主要碎片。或者A=2-甲基-1,3-丁二烯(异戊二烯)CH2=C(CH3)CH=CH2:臭氧→HCHO + CH3COCHO(丙酮醛)+ HCHO。也不完全符合。
最合理:A = 1,4-戊二烯,若按每个双键独立臭氧分解:每个末端烯各给HCHO,中间碳给二醛。但题目说"甲醛+丙醛"→可能题意是还原性臭氧分解(Zn处理)后合并碎片。修正答案仍为1,3-戊二烯。
(b) C6H10,DBE=(12+2-10)/2=2。过量H2→环己烷(有环!)→1个环+1个不饱和度(C=C或C≡C)。
Lindlar加1eq H2→C6H12(仍DBE=1=环)→加的这1eq H2把C≡C变成C=C!
所以B含有一个三键+一个环...不对,Lindlar加1eq H2→三键变双键(DBE从2→1)。最终加氢→环己烷=只有环。
答:B = 环己炔(cyclohexyne)? 但环己炔极不稳定(环内三键张力大)。
或:B含一个环+一个C≡C在侧链? 但加氢得环己烷意味着无侧链碳。C6H10加氢→C6H12(环己烷)→增加了1个H2(Lindlar)再加1个H2=总2个H2→原来有三键(加2H2→单键)。含6C成环+三键在环上→B = 环己炔。虽然不稳定,但这是逻辑推断结果。
推断题策略:从分子式算DBE→加氢实验确定不饱和度类型→碎片分析确定位置。
题6 合成路线
题6
(a) 从乙炔和任何碳数≤2的有机物,合成2-己炔。
(b) 从1,3-丁二烯和合适的亲二烯体,合成4-环己烯-1,2-二甲酸(cis)。
解题思路:(a)炔的碳链增长=炔负离子烷基化(SN2,限用1°RX)。(b)DA反应→顺式双酸。
(a) 合成2-己炔 CH3C≡CCH2CH2CH3:
逆推:2-己炔 ← 1-丁炔− + CH3CH2Br(或丙炔− + 正丙基溴→但正丙基溴是1°✓)
路线一:
HC≡CH + NaNH2 → HC≡C−Na+
HC≡C− + CH3CH2Br → CH3CH2C≡CH(1-丁炔)
1-丁炔 + NaNH2 → CH3CH2C≡C−Na+
CH3CH2C≡C− + CH3CH2Br → CH3CH2C≡CCH2CH3(3-己炔?)
注意:要得2-己炔(CH3C≡C-C3H7),需:
HC≡CH + NaNH2 → HC≡C− + CH3Br → CH3C≡CH(丙炔)
丙炔 + NaNH2 → CH3C≡C− + CH3CH2CH2Br(正丙基溴,1°) → CH3C≡CCH2CH2CH3(2-己炔) ✓
但正丙基溴是C3试剂>C2。如果限制≤C2:
HC≡C− + C2H5Br → 1-丁炔 → 1-丁炔− + C2H5Br → 3-己炔(不是2-己炔)。
需要CH3Br: HC≡C− + CH3Br → 丙炔 → 丙炔− + C2H5Br → 2-戊炔(5C)。还差一个C。
答:用两步烷基化:HC≡C− + CH3Br → 丙炔− + CH3CH2Br → 2-戊炔(C5)。若需C6则需C3试剂。题目"碳数≤2"可能指每个试剂≤C2,无法直接得到2-己炔(需要正丙基卤)。修改目标为3-己炔则可行。
(b) 合成cis-4-环己烯-1,2-二甲酸:
DA反应:1,3-丁二烯(二烯) + 马来酸酐(cis-亲二烯体) → 环己烯-4,5-二甲酸酐
→ 水解酸酐 → cis-4-环己烯-1,2-二甲酸 ✓
关键:马来酸酐中两个C=O为cis→DA反应syn加成→产物中两个COOH保持cis关系。若用反丁烯二酸(fumaric acid)→得trans二酸。
DA反应的立体专一性:亲二烯体的cis取代基在产物中保持cis(endo或exo面)。这是syn[4+2]环加成的必然结果。


