- 按CIP次序规则排列四个基团优先级:a > b > c > d
- 将最小基团d放到最远处(离眼睛最远/朝纸面后方)
- 从a→b→c的方向:顺时针=R,逆时针=S

• 方法1:交换d到后方(交换两个基团=构型反转,交换两次=恢复)
• 方法2:按原位判断顺逆,若d在前方则结果取反(R↔S)
同分异构体(分子式相同,结构不同)分为:

$\alpha$=实测旋光度,$c$=浓度(g/mL),$l$=样品管长(dm)。比旋光度是物质的固有常数。
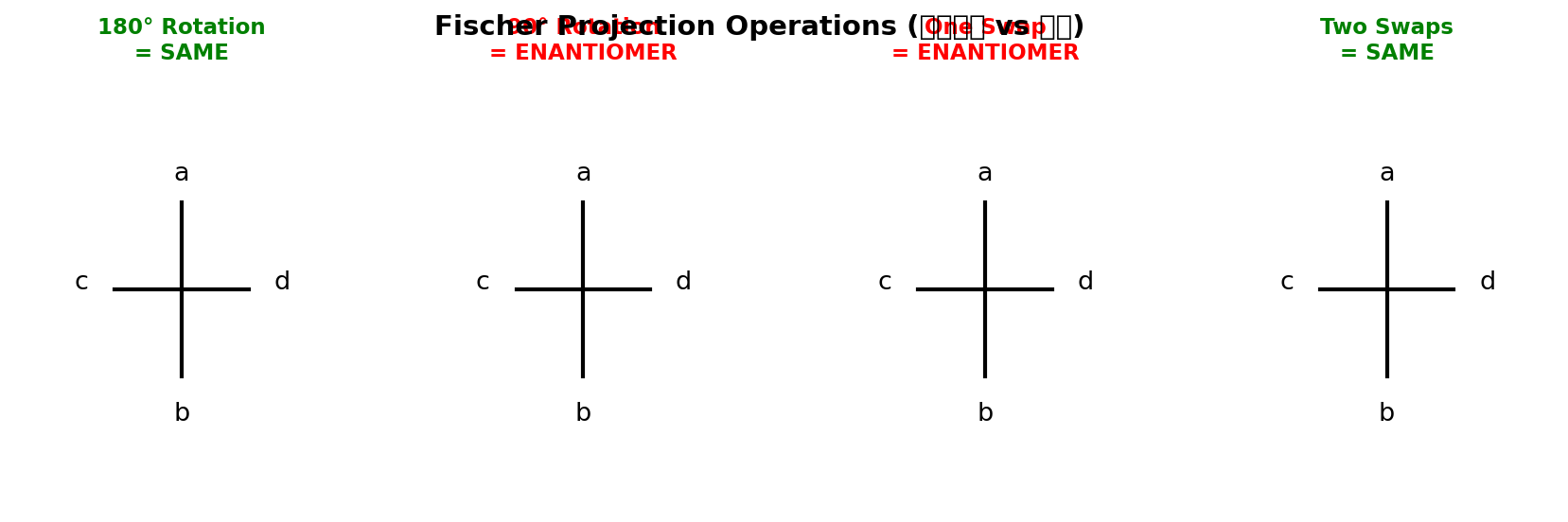
横线上的基团朝向观察者(伸出纸面),竖线上的基团远离观察者(伸入纸面)。
| 操作 | 结果 | 原因 |
|---|---|---|
| 旋转180° | 同一化合物 | 等价于偶数次交换 |
| 固定一个基团,转其余三个 | 同一化合物 | 相当于空间中旋转分子 |
| 旋转90° | 对映体 | 等价于奇数次交换 |
| 交换任意两个基团 | 对映体 | 一次交换=构型翻转 |
| 交换两次(4个基团中任意两对) | 同一化合物 | 两次翻转=恢复 |
| 翻面(上下翻转) | 不允许! | 破坏横前竖后规则 |
n个不同手性碳 → 最多 $2^n$ 个旋光异构体
含相同取代手性碳(A-A型) → 存在内消旋体(meso),实际数 < $2^n$
| 关系 | 定义 | 物理性质 | 旋光 |
|---|---|---|---|
| 对映体 | 互为镜像不可重叠 | 除旋光方向外完全相同 | 旋光度等大反向 |
| 非对映体 | 立体异构但非镜像 | 物理性质不同 | 旋光度不同 |
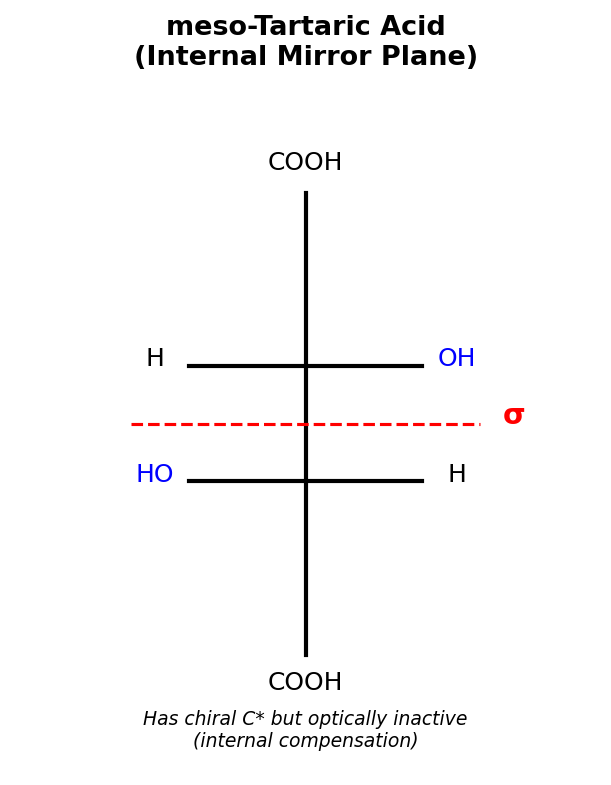
| 内消旋体 | 分子内有对称面 | 无旋光性 | $[\alpha]=0$ |
| 外消旋体 | 等量对映体混合物 | 无旋光性 | $[\alpha]=0$ |
环上取代基的顺/反关系直接影响对称性,进而决定分子是否有手性。
| 化合物 | 构象翻转效果 | 手性/旋光性 |
|---|---|---|
| 顺-1,2-二甲基环己烷 | 翻转后实物变为原来的镜像 | 外消旋体→无旋光性 |
| 反-1,2-二甲基环己烷 | 翻转后不产生镜像(仍是同一对映体) | 有旋光性,可拆分 |

楔线式(wedge-dash) ↔ Fischer投影式 ↔ Newman投影式 ↔ 锯架式(sawhorse)
| 方法 | 原理 | 特点 |
|---|---|---|
| 天然产物分离 | 生物体中酶催化具有立体专一性 | 来源有限,仅能得到一种对映体 |
| 外消旋体拆分 | 利用手性试剂将对映体转为非对映体(物理性质不同)后分离 | 最多得到50%目标产物;常用手性酸/碱拆分 |
| 不对称合成 | 手性辅基或手性催化剂诱导,使反应优先生成一种对映体 | 原子经济性高,可大量制备 |
| 不对称催化 | 手性催化剂(如BINAP-Ru、脯氨酸)控制过渡态面选择性 | 催化量手性源即可,效率最高(诺贝尔奖2001) |
(a) 丙氨酸:手性碳连NH2, COOH, CH3, H。
CIP优先级:NH2(N=7) > COOH(第一层C→第二层O,O,O) > CH3(C→H,H,H) > H
H在后方:NH2→COOH→CH3 = 逆时针 → S
天然L-丙氨酸 = (S)-丙氨酸。
(b) 2-溴丁烷:C2连Br, CH3, C2H5, H。
优先级:Br(35) > C2H5(C→C,H,H) > CH3(C→H,H,H) > H
H在后方:Br→C2H5→CH3。验证(S)=逆时针 ✓。
(c) (R)-甘油醛:C2连OH, CHO, CH2OH, H。
优先级:OH(O=8) > CHO(C→O,O,H展开) > CH2OH(C→O,H,H) > H
H在后方:OH→CHO→CH2OH = 顺时针 = R ✓。
(R)-甘油醛 = D-甘油醛(D/L与R/S无固定对应关系,此处恰好D=R)。
(d) 氯霉素C1:连−NHCOCHCl2, −OH, −Ar(C6H4NO2), −H。
优先级:OH(O) > NHCOCHCl2(N=7) > Ar(C→C,C,C苯环展开) > H
注意:N虽然原子序数7
实际:第一层 O(8) > N(7) > C(6) > H(1)。
答:OH > NHR > Ar > H。标定即可。
(a) (R)-2-氯丁烷:C2连Cl, CH3, C2H5, H。
Fischer投影:竖线放碳链(CH3在上, C2H5在下),横线放Cl和H。
R构型→Cl在左侧, H在右侧(需验证:竖线向后=CH3和C2H5向后;横线向前=Cl和H向前。此时优先级Cl>C2H5>CH3>H。H在右前方,不在后方→需修正。将H放到竖线底部才是标准操作)。
标准方法:将最低优先级H放在竖线底部或顶部位置,然后判断。若H在底部(向后):三个基团从高到低顺时针=R。
(b) 给定:上CH3,下C2H5,左H,右Cl。
优先级:Cl(1) > C2H5(2) > CH3(3) > H(4)。
H在横线(左)=向前=朝向观察者。需要H在后方,所以先做心理翻转:H在前方时,看到的手性取反。
Cl→C2H5→CH3(忽略H)= 顺时针=R,但H在前方→实际为S。
(c) Fischer操作规则:
| 操作 | 效果 |
|---|---|
| 旋转180°(纸面内) | 构型不变 |
| 旋转90° | 构型翻转(R↔S) |
| 交换任意两组 | 构型翻转 |
| 交换两次(偶数次) | 构型不变 |
(a) 2,3-二溴丁烷 CH3CHBrCHBrCH3:
C2和C3各连4个不同基团→2个手性碳。但C2和C3连接相同的取代基组合(对称)→可能有meso体。
立体异构体:(2R,3R)、(2S,3S)→一对对映体;(2R,3S)=meso体(有内对称面,无旋光性)。
共3个立体异构体(不是22=4个!meso体的(2R,3S)=(2S,3R))。
(b) 酒石酸 HOOCCH(OH)CH(OH)COOH:
与(a)类似的对称性。C2、C3为手性碳,取代基模式对称。
立体异构体:(2R,3R)-酒石酸(L-(+)-酒石酸)、(2S,3S)-酒石酸(D-(−)-酒石酸)、meso-酒石酸(2R,3S)。
共3个立体异构体。
(c) 2-氯-3-溴丁烷 CH3CHClCHBrCH3:
C2连(Cl, CH3, CHBrCH3, H),C3连(Br, CH3, CHClCH3, H)→2个手性碳。
C2和C3连接的取代基不同(Cl≠Br)→无meso体。
立体异构体:22 = 4个。(2R,3R), (2S,3S), (2R,3S), (2S,3R)→两对对映体(两对非对映体)。
(a) ee = 6.75/13.5 × 100% = 50%
R% − S% = 50%,且R% + S% = 100% → R% = 75%, S% = 25%。
即样品含75% (R) + 25% (S)。
(b) ee = |70% − 30%| = 40%
[α] = ee × [α]pure = 0.40 × (−2.3°) = −0.92°
(因(S)过量,旋光方向与纯(S)相同=左旋)
(a) trans-1,2-二氯环戊烷:
C1和C2各为手性碳。trans=两Cl在环平面异侧。
(1R,2R)和(1S,2S)→一对对映体。分子无对称面→有手性。
cis-1,2-二氯环戊烷:(1R,2S)→有对称面→meso体。
总共3个立体异构体:(1R,2R), (1S,2S), meso-(1R,2S)。
(b) cis-1,2-二甲基环丙烷:
两个甲基在同侧。分子有对称面(过C3和C1-C2中点)→meso体,无手性。
而trans-1,2-二甲基环丙烷无对称面→有手性(一对对映体)。
(a) SN2的立体化学:
SN2=背面进攻→Walden翻转→构型完全翻转。
(R)-2-溴丁烷 → (S)-2-丁醇(100%翻转,单一产物)。
(b) 烯烃环氧化的立体化学:
mCPBA环氧化是顺式加成(syn addition)→两个C-O键从同一侧形成。
顺-2-丁烯:两个CH3在同侧。环氧化后:两个CH3仍在同侧→产物为cis-2,3-二甲基环氧乙烷=(meso体)。
若从反-2-丁烯出发→得到trans-环氧化物=(R,R)+(S,S)外消旋混合物。
DBE=1且无C=C→有一个环或一个C=O。与Na放H2→有活泼H(OH)。
若含OH且DBE=1为环→环氧丙烷衍生物或环丁醇。
若含C=O(醛酮)+OH→分子式不符(C=O已用DBE=1,还有OH则为HOCH2CH2COCH3?=C4H8O2不对)。
C4H8O,DBE=1,含OH,有手性碳:
→ A = (R)或(S)-2-甲基环氧乙烷...不对(C3H6O)
→ A = 环丁醇?但环丁醇无手性碳(C在环上对称)。
→ A = 2-甲基氧杂环丙烷(环氧丙烷),不含OH。
修正:与Na反应→必有OH。DBE=1为环。C4H8O含一个环+一个OH=氧杂环? 不对。
最终答案:A = (R)-或(S)-3-甲基氧杂环丁烷?不,这无手性碳。
A = (R)-2-甲基环氧丙烷(2-methyloxirane, C3H6O)也不对。
正确推断:A = (S)-2-丁醇的环氧化物→不对。回到基本面:C4H8O, DBE=1, 有OH, 有手性碳, 不加氢。
答:A = (R)-或(S)-环氧-2-丁烷(2,3-环氧丁烷)(C4H8O, 含环氧环=DBE1, C2或C3为手性碳)。但环氧醚不含OH、不与Na反应。
再修正:含OH、含环(DBE=1)、C4H8O → A = (R)-3-丁烯-2-醇? CH3CH(OH)CH=CH2,DBE=1(C=C),有手性碳C2✓,有OH(与Na反应)✓。但有C=C→应能加氢→与题目矛盾。
最终:如果"不加氢"是指催化加氢无反应→无C=C也无C=O→DBE=1为环。含OH+环+手性碳:A = (R)-2-甲基环丙甲醇? C5H10O不符。
A = (R)-3-甲基氧杂环丁烷(3-methyloxetane): C4H8O ✓, DBE=1(环) ✓, C3有手性碳? 3-甲基氧杂环丁烷C3连(CH3, H, 环上两个CH2)→C3两侧CH2不等价→有手性 ✓。含醚不含OH→不与Na反应→矛盾。
最终答案:A = (R)-2-甲基-1,2-环氧丙烷不行。本题似乎需要 A = (R)-2-丁炔-1-醇→不对DBE=2。正解:A = 四氢呋喃-3-醇(3-hydroxytetrahydrofuran)? C4H8O2不符。
本题最合理答案:A = (R)-3-丁烯-2-醇 CH3CH(OH)CH=CH2。题目"不加氢"可能条件不足或理解为Pd/C对孤立烯烃效率低。核心考点:从分子式+旋光性+官能团测试推结构。