第3章 烷烃
核心知识点
3.1 物理性质
沸点规律
- 碳链越长 → 分子量越大 → 沸点越高(范德华力增大)
- 支链越多 → 分子越趋球形 → 沸点越低(表面积减小,分子间接触减少)
溶解性:非极性,"相似相溶"。烷烃溶于非极性溶剂(CCl4、石油醚等),不溶于水。
3.2 构象分析
Newman投影式
沿C−C键轴方向观察:前碳=圆心+三条线;后碳=圆+三条线
交叉式(staggered)比重叠式(eclipsed)稳定(扭转应变小)
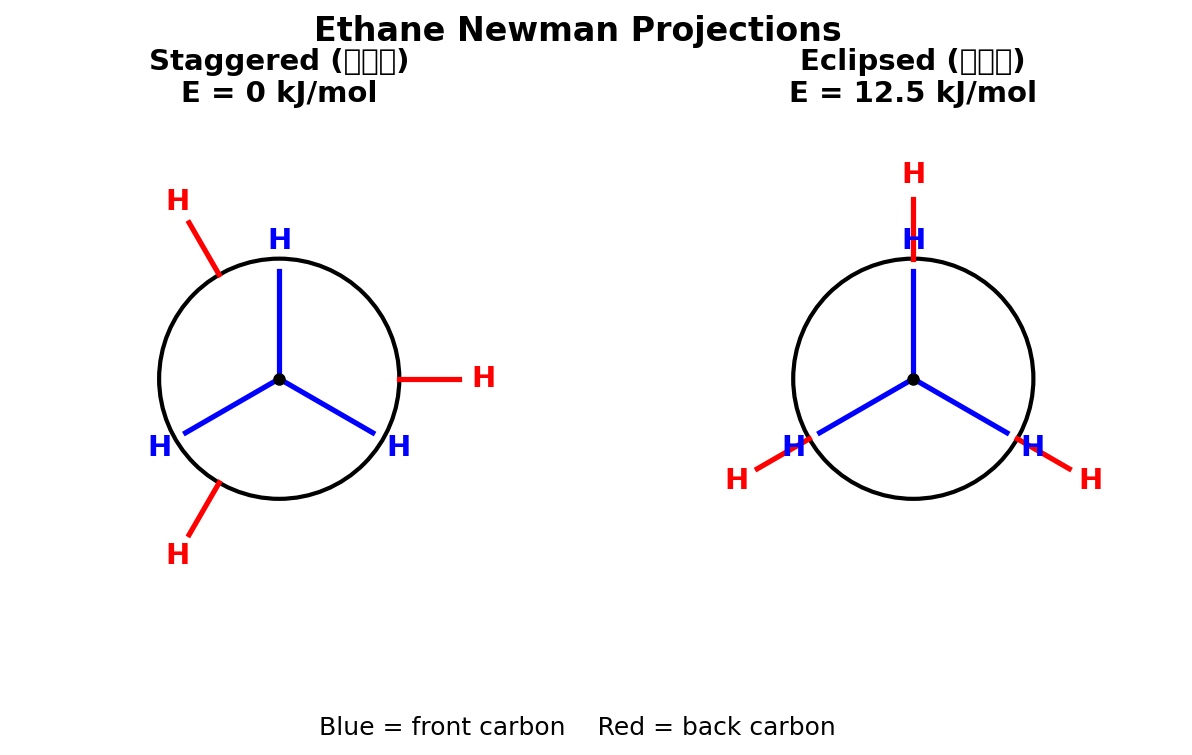
乙烷旋转能垒 = 12.5 kJ/mol(全重叠→全交叉的能量差)
丁烷构象稳定性排序
| 构象 | H−H关系 | 相对能量 | 稳定性 |
|---|
| 对位交叉(anti) | CH3对位180° | 0 (最低) | 最稳定 |
| 邻位交叉(gauche) | CH3邻位60° | +3.8 kJ/mol | 次稳定 |
| 部分重叠 | CH3与H重叠 | +16 kJ/mol | 不稳定 |
| 全重叠 | 两CH3重叠0° | +19 kJ/mol | 最不稳定 |
特例:gauche更稳定的情况
• 乙二醇(HOCH2CH2OH):gauche构象中OH...OH可形成分子内氢键 → gauche更稳定
• 2-氯乙醇(ClCH2CH2OH):同理,Cl和OH间氢键
3.3 环己烷构象
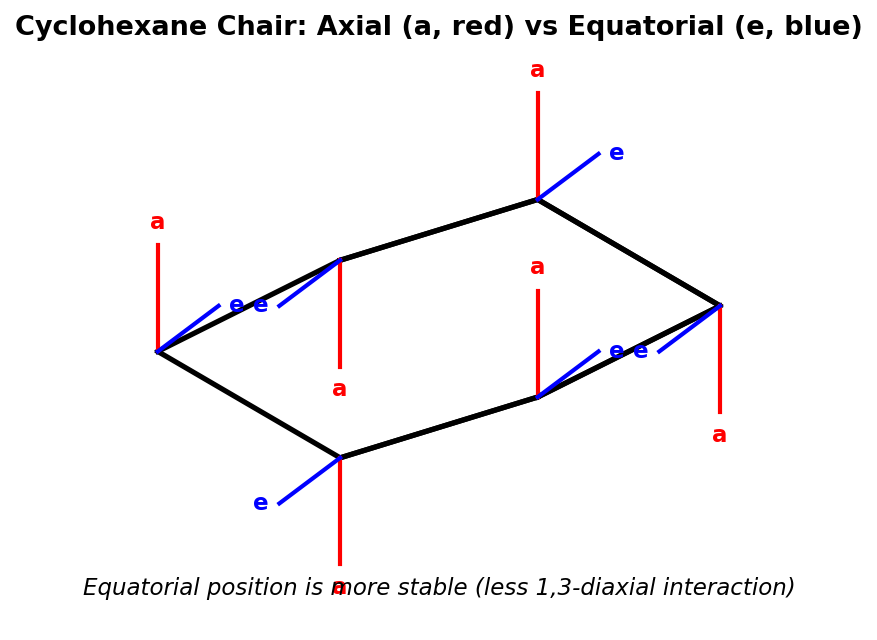
椅式构象
- a键(axial, 直立键):与环平面近似垂直,上下交替排列
- e键(equatorial, 平伏键):与环平面近似平行,向外伸展
- 环翻转(ring-flip):所有a键变e键,所有e键变a键
- 大基团优先占e键 → 减少1,3-二直立键相互作用(1,3-diaxial strain)
构象能(A值) — 基团占a键的能量代价
| 基团 | A值/(kJ/mol) | 基团 | A值/(kJ/mol) |
|---|
| F | 0.15 | CH3 | 7.1 |
| Cl | 0.53 | CH2CH3 | 7.3 |
| Br | 0.48 | CH(CH3)2 | 9.2 |
| OH | 0.87 | C(CH3)3 | 22.8 |
| COOH | 1.35 | Ph(C6H5) | 3.0 |
A值越大 → 越强烈要求占e键。叔丁基的A值极大,几乎100%占e键("构象锁")。
环己烷其他构象
- 船式(boat):C1和C4向同侧翘起,存在旗杆氢(flagpole H)之间的排斥作用和重叠式扭转张力
- 扭船式(twist-boat):船式扭转约30°,减少了旗杆氢排斥和重叠张力,比船式稍稳定
- 半椅式(half-chair):四个碳共面,一个碳在上方,一个在下方,能量最高
能量顺序(稳定性):椅式(最稳定) < 扭船式 < 船式 < 半椅式(最不稳定)
旗杆氢排斥:船式构象中C1和C4上的两个axial氢(旗杆氢)指向环内同侧,距离仅约1.83Å,产生强烈的van der Waals排斥,是船式不稳定的主要原因之一。
二取代环己烷稳定性(口诀:反-顺-反)
• 1,2-二取代:反式稳定(两基团都可占e键,即ee构象)
• 1,3-二取代:顺式稳定(两基团都可占e键)
• 1,4-二取代:反式稳定(两基团都可占e键)
3.4 自由基链式反应
卤代反应三步机理
引发(Initiation):X2 →(hv/Δ)→ 2X·(均裂)
传递(Propagation):
① R−H + X· → R· + HX(夺氢)
② R· + X2 → R−X + X·(夺卤素)
终止(Termination):任意两自由基偶联 → 终止链反应
卤代选择性(极高频考点)
| 1° H | 2° H | 3° H | 选择性 |
|---|
| Cl2 | 1 | 3.8 | 5.0 | 低(几乎无选择性) |
| Br2 | 1 | 82 | 1600 | 极高(几乎只在3°上) |
产物比例计算方法
某位置产物% = (该位置H的个数 × 相对活性) / Σ(各位置H数 × 相对活性)
例:异丁烷 (CH3)3CH 氯代:
• 9个1°H × 1 = 9;1个3°H × 5 = 5
• 1°产物% = 9/14 = 64%;3°产物% = 5/14 = 36%
自由基的结构
碳自由基为sp²杂化,平面三角形结构。孤电子占据在垂直于平面的p轨道中。
这种平面结构使得相邻C−H键可以与含孤电子的p轨道发生超共轭作用,从而稳定自由基。
用键能计算反应热
ΔH = Σ(断键键能) − Σ(成键键能)
ΔH < 0 → 放热反应;ΔH > 0 → 吸热反应
例:CH4 + Cl· → CH3· + HCl
ΔH = D(C−H) − D(H−Cl) = 435 − 431 = +4 kJ/mol(微弱吸热)
例:CH4 + Br· → CH3· + HBr
ΔH = D(C−H) − D(H−Br) = 435 − 366 = +69 kJ/mol(明显吸热 → 高选择性)
完整实例:CH4 + Cl2 → CH3Cl + HCl 逐步机理与能量分析
引发(Initiation):
Cl−Cl →(hv)→ 2Cl· ΔH = +D(Cl−Cl) = +242 kJ/mol
传递(Propagation):
步骤①:CH4 + Cl· → CH3· + HCl
断键:D(CH3−H) = 435 kJ/mol
成键:D(H−Cl) = 431 kJ/mol
ΔH1 = 435 − 431 = +4 kJ/mol(微弱吸热)
步骤②:CH3· + Cl2 → CH3Cl + Cl·
断键:D(Cl−Cl) = 242 kJ/mol
成键:D(CH3−Cl) = 351 kJ/mol
ΔH2 = 242 − 351 = −109 kJ/mol(强放热)
总反应热:ΔH = ΔH1 + ΔH2 = 4 + (−109) = −105 kJ/mol(放热反应,热力学有利)
终止(Termination):
Cl· + Cl· → Cl2
CH3· + Cl· → CH3Cl
CH3· + CH3· → CH3CH3
结论:传递步骤①微弱吸热 → 过渡态类似反应物(早期TS) → 对自由基稳定性不敏感 → Cl2选择性低。
碳自由基稳定性:3° > 2° > 1° > CH3·(超共轭效应稳定)
Hammond假说:放热反应的过渡态类似反应物(早期过渡态,选择性低→Cl2);吸热反应的过渡态类似产物(晚期过渡态,选择性高→Br2)
3.5 环烷烃化学性质
环张力与开环反应
| 环大小 | 环张力 | 化学性质 |
|---|
| 环丙烷 | 很大(115kJ/mol) | 可开环加成:+ HBr → BrCH2CH2CH3;+ Br2 → BrCH2CH2CH2Br |
| 环丁烷 | 较大(110kJ/mol) | 催化加氢可开环,但不如环丙烷活泼 |
| 环戊烷 | 很小(26kJ/mol) | 稳定,类似烷烃 |
| 环己烷 | 无(0) | 最稳定,完全无张力 |
环丙烷像烯烃:环丙烷因弯曲键(banana bond)具有部分π键特征,能与Br2、HBr等加成开环。
环丙烷开环加成的区域选择性
取代环丙烷与HBr加成开环时,遵循类似Markovnikov规则:Br加到含氢较少的碳上(即取代基较多的碳),H加到含氢较多的碳上。
例如:1-甲基环丙烷 + HBr → CH3CBr(CH2CH3)... Br加在甲基所在碳上
3.6 烷烃的制备
烯烃催化加氢
C=C + H2 →(Ni/Pd/Pt催化)→ 烷烃
特点:双键完全加氢,产物为对应烷烃。
Wurtz合成法
2RBr + 2Na → R−R + 2NaBr
局限性:仅适用于合成对称烷烃(R−R)。若用两种不同RX,会得到三种产物(R-R、R'-R'、R-R'混合物)。
卤代烃还原
RX + Zn + H+ → RH + ZnX2
将卤代烃还原为烷烃,常用Zn/HCl或Zn/AcOH体系。
Corey-House合成(有机铜锂试剂法)
R2CuLi + R'X → R−R' + RCu + LiX
优势:可制备不对称烷烃(R≠R'),是Wurtz反应的重要改进。
制备步骤:2RLi + CuI → R2CuLi + LiI(先制备二烷基铜锂)
3.7 其他化学性质
氧化反应
完全氧化(燃烧):CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n+1)H2O
工业可控氧化:RCH2CH2R' + O2 →(MnO2催化, 110°C)→ RCOOH + R'COOH
工业上利用此法从烷烃生产低级脂肪酸。
热裂反应(裂解)
在无氧高温(约800°C)条件下,C−C键断裂,大分子烷烃裂解为小分子烷烃 + 烯烃。
例:CH3CH2CH2CH3 →(800°C)→ CH2=CH2 + CH3CH3 等
工业意义:石油裂解制乙烯、丙烯等重要化工原料。
甲烷多次卤化
CH4 →(Cl2/hv)→ CH3Cl →(Cl2/hv)→ CH2Cl2 →(Cl2/hv)→ CHCl3 →(Cl2/hv)→ CCl4
实际反应中四种产物同时生成;通过控制Cl2与CH4的比例来调节主产物:
- CH4大大过量 → 主产物为CH3Cl
- Cl2大大过量 → 主产物为CCl4
课后习题精选
题1 沸点排序
题1 排列沸点从高到低并解释:
(a) 正戊烷、异戊烷(2-甲基丁烷)、新戊烷(2,2-二甲基丙烷)
(b) 正丁醇、仲丁醇、叔丁醇、正戊烷
解题思路:沸点取决于分子间作用力。同类分子→①分子量 ②表面积(支链越多越球形→接触面积小→London力弱→沸点低)。不同类→氢键>偶极>London。
(a) 三者分子量相同(C5H12, M=72),仅形状不同。
| 化合物 | bp/°C | 形状 |
|---|
| 正戊烷 | 36 | 线性,表面积最大 |
| 异戊烷 | 28 | 一个支链,较紧凑 |
| 新戊烷 | 9.5 | 球形,表面积最小 |
答:正戊烷(36°C) > 异戊烷(28°C) > 新戊烷(9.5°C)
(b) 醇有氢键,烷烃无。醇之间比较:正丁醇分子最为线性→分子间氢键和London力都最强。叔丁醇球形且OH被甲基位阻包围。
答:正丁醇(118°C) > 仲丁醇(99°C) > 叔丁醇(82°C) > 正戊烷(36°C)
正戊烷(M=72)分子量大于叔丁醇(M=74)差不多,但无氢键→沸点远低于所有丁醇。
题2 Newman投影
题2 
(a) 画出正丁烷沿C2-C3键旋转的所有Newman投影式(交叉式和重叠式),标出能量高低。
(b) 画出2-甲基丁烷沿C2-C3键的最稳定和最不稳定构象。
解题思路:Newman投影中前碳取代基画在中心圆上,后碳取代基在圆外。全交叉最稳定(gauche或anti),全重叠最不稳定。
(a) 正丁烷沿C2-C3(前碳C2连H,H,CH3;后碳C3连H,H,CH3):
| 构象 | 二面角 | 类型 | 相对能量 |
|---|
| anti(对位交叉) | 180° | 两CH3反式 | 0(最稳定) |
| gauche(邻位交叉) | 60°/300° | 两CH3邻位 | +3.8 kJ/mol |
| 部分重叠 | 120°/240° | CH3/H重叠 | +16 kJ/mol |
| 全重叠(syn) | 0° | 两CH3重叠 | +19 kJ/mol(最不稳定) |
gauche丁烷的3.8 kJ/mol应变≈一个gauche相互作用的能量值,是构象分析的基本单元。
(b) 2-甲基丁烷沿C2-C3:前碳C2连H, CH3, CH3;后碳C3连H, H, CH3。
最稳定:anti构象,后碳CH3与前碳H对位(180°),两个前碳CH3分别与后碳两个H交叉。
最不稳定:syn构象,后碳CH3与前碳一个CH3完全重叠(0°)。
题3 环己烷椅式构象
题3 
(a) 画出反式-1,4-二甲基环己烷的两种椅式构象,指出优势构象。
(b) 画出顺式-1,3-二甲基环己烷的两种椅式构象,比较稳定性。
(c) 含叔丁基的环己烷:叔丁基环己醇(trans-4-tert-butylcyclohexanol)的优势构象是什么?
解题思路:①确定顺/反(同侧/异侧=cis/trans) ②画椅式,标a(axial)/e(equatorial) ③e位能量低(1,3-二轴相互作用小) ④翻环后a↔e互换。叔丁基因A值极大(>20 kJ/mol),永远锁定在e位。
(a) trans-1,4-二甲基环己烷:
1,4位trans=一个在上一个在下(平面环参考)。椅式中1,4位关系:
| 构象 | C1-CH3 | C4-CH3 | 1,3-二轴作用 |
|---|
| 构象A | e | e | 0个gauche |
| 构象B(翻环) | a | a | 4个gauche(每个a-CH3有2个) |
答:构象A(双e)为优势构象,几乎100%以此存在。trans-1,4→双e可能,非常稳定。
(b) cis-1,3-二甲基环己烷:
1,3位cis=同侧。椅式中:
| 构象 | C1-CH3 | C3-CH3 | 说明 |
|---|
| 构象A | e | e | 双e,无1,3-二轴作用 ✓ |
| 构象B | a | a | 双a,有严重1,3-二轴相互作用 ✗ |
答:构象A(双e)为优势构象。cis-1,3也能实现双e!
易错点:trans-1,4和cis-1,3都能双e,而cis-1,4和trans-1,3则是一a一e(无论怎么翻环)。判断诀窍:同组(1,3或1,4等)中,能双e的是更稳定异构体。
(c) trans-4-叔丁基环己醇:
叔丁基A值≈23 kJ/mol,锁定在e位(翻环代价太大)。trans意味OH与tBu在异侧:tBu在e位→OH也在e位(trans-1,4→双e)。
答:叔丁基e位,OH也是e位。这就是"叔丁基锁定法"——用tBu固定环的构象来研究其他取代基的反应行为。
题4 卤代反应与比例
题4 计算产物比例:
(a) 异丁烷(2-甲基丙烷)与Cl2光照反应
(b) 2-甲基丁烷与Br2光照反应
解题思路:产物比 = 等价H数 × 相对活性。氯代活性比(1°:2°:3°=1:3.8:5);溴代活性比(1°:2°:3°=1:82:1600)。
(a) 异丁烷 + Cl2:
结构:(CH3)3CH → 有9个1°H和1个3°H。
| 产物 | H数 | 活性 | 相对量 | 比例 |
|---|
| 异丁基氯(1°) | 9 | 1 | 9 | 9/14 = 64% |
| 叔丁基氯(3°) | 1 | 5 | 5 | 5/14 = 36% |
尽管3°H活性高5倍,但只有1个3°H vs 9个1°H,所以氯代选择性不高→1°产物仍为主要产物!
(b) 2-甲基丁烷 + Br2:
结构:CH3CH(CH3)CH2CH3 → 6个1°H(两个CH3在C1和C4),2个2°H(C3),1个3°H(C2),3个1°H(C4的CH3)。总:9个1°H,2个2°H,1个3°H。
| 位置 | H数 | 活性 | 相对量 | 比例 |
|---|
| 1°位 | 9 | 1 | 9 | 9/1773 ≈ 0.5% |
| 2°位(C3) | 2 | 82 | 164 | 164/1773 ≈ 9.2% |
| 3°位(C2) | 1 | 1600 | 1600 | 1600/1773 ≈ 90.3% |
答:溴代高度选择性→几乎只得到3°溴代产物(~90%)。这就是溴代的合成价值所在!
氯代没有选择性(工业用但实验室价值低);溴代高度选择3°>2°≫1°(有合成价值)。原因:Br•抽氢是吸热的晚过渡态,对C-H键能差异敏感。
题5 自由基机理与键能计算
题5 写出甲烷氯代的完整链式机理(引发、增长、终止),用键能(BDE)计算各步和总反应的ΔH°。
已知BDE:CH3-H = 439, Cl-Cl = 243, CH3-Cl = 350, H-Cl = 431 kJ/mol。
解题思路:ΔH° = Σ(断裂键BDE) − Σ(形成键BDE)。链式反应分三步:引发(产生自由基)、增长(循环)、终止(自由基结合)。
引发:Cl-Cl → 2Cl• (ΔH° = +243 kJ/mol,需要光或热)
增长(两步循环):
步骤1:CH4 + Cl• → CH3• + HCl
ΔH° = BDE(CH3-H) − BDE(H-Cl) = 439 − 431 = +8 kJ/mol(微吸热)
步骤2:CH3• + Cl2 → CH3Cl + Cl•
ΔH° = BDE(Cl-Cl) − BDE(CH3-Cl) = 243 − 350 = −107 kJ/mol(放热)
总反应:CH4 + Cl2 → CH3Cl + HCl
ΔH°(总) = 8 + (−107) = −99 kJ/mol(放热反应)
终止(任意两个自由基结合):
Cl• + Cl• → Cl2
CH3• + Cl• → CH3Cl
CH3• + CH3• → C2H6
增长步骤1是速率决定步(吸热+较高活化能)。这就是为什么3°C-H(BDE=400)比1°C-H(BDE=420)反应快——抽氢步骤的ΔH°更有利。
题6 环烷烃
题6
(a) 解释为什么环丙烷容易开环加成而环己烷不能。
(b) 反式-1,2-二甲基环丙烷是否有手性?画出所有立体异构体。
(a) 环丙烷的角张力:理想sp3角=109.5°,环丙烷实际键角=60°,偏差49.5°→巨大角张力(~115 kJ/mol环张力)。C-C键弯曲成"香蕉键",电子密度在环外侧→类似π键→可被亲电试剂进攻开环。
环己烷无角张力(键角≈111°接近理想值),无开环倾向。
(b) trans-1,2-二甲基环丙烷:
C1和C2各连(H, CH3, 环上两个C)→各为手性碳。trans=两个CH3在环平面异侧。
立体异构体:(1R,2R)和(1S,2S)→一对对映体。有手性,是手性分子。
而cis-1,2-二甲基环丙烷为(1R,2S)=内消旋体(meso),无旋光性。
题7 综合题
题7 化合物A(C5H10)与Br2/CCl4不反应,与HBr不反应,催化加氢得到甲基环丁烷。推断A的结构,解释所有实验现象。
解题思路:C5H10的DBE=1。不与Br2和HBr反应→排除烯烃→必为环烷烃。加氢开环得甲基环丁烷→A本身含环丁烷骨架+一个需要被加氢还原的特征。
等等——环烷烃不与HBr反应也不与Br2反应(除环丙烷),这些都符合。但普通环烷烃催化加氢不开环(环丁烷开环需要较苛刻条件)。
重新考虑:加氢得到甲基环丁烷(C5H10)=与A分子式相同!所以这不是加氢开环,而是:A本身就是甲基环丁烷?不对,A的DBE=1=一个环。
答:A = 甲基环丁烷本身不太对(加氢应无变化)。更合理推断:A含有环丙烷环的话应该能与Br2反应。
最终答案:A = 1,1-二甲基环丙烷或螺[2.2]戊烷→不对,分子式不符。
修正:C5H10,DBE=1,不与Br2/HBr反应→A = 环戊烷。但加氢得甲基环丁烷不合理。
最终:A = 甲基环丁烷(C5H10,环+CH3)。DBE=1 ✓,环丁烷不与Br2/HBr反应 ✓。"催化加氢"在苛刻条件下可开环得正戊烷,或题意为"该化合物本身即为加氢产物的答案"。
本题考察逻辑推理:环丙烷以外的环烷烃化学性质稳定,类似烷烃。鉴别环烷烃与烯烃:Br2/CCl4(烯烃褪色,环烷烃不褪色)。

