第2章 脂肪(环)烃的结构与命名
核心知识点
2.0 烃的分类体系
烃的分类总览
- 烃(碳氢化合物)
- 脂肪烃(开链烃)
- 环烃
- 脂环烃(饱和:环烷烃;不饱和:环烯烃等)
- 芳香烃(苯及其衍生物)
2.1 碳原子的杂化
| 杂化类型 | 轨道组成 | 几何构型 | 键角 | 键类型 | 实例 |
|---|
| $sp^3$ | 1s+3p | 四面体 | 109.5° | 4个σ键 | CH4、烷烃 |
| $sp^2$ | 1s+2p | 平面三角 | 120° | 3σ+1π | CH2=CH2、苯 |
| $sp$ | 1s+1p | 直线 | 180° | 2σ+2π | HC≡CH、CO2 |
σ键 vs π键
- σ键:头对头重叠,可自由旋转,键能高,键稳定
- π键:肩并肩重叠,不可旋转(旋转会破坏),活性大,易发生加成
键长与键能
| 键 | 键长/pm | 键能/(kJ/mol) |
|---|
| C−C | 154 | 347 |
| C=C | 134 | 611 |
| C≡C | 121 | 837 |
键越短 → 键能越大 → 键越强 → 但π键部分活性高
杂化判断口诀:看该原子连接的"基团数"(包括孤电子对计为一个基团):4个→sp3,3个→sp2,2个→sp。
2.2 共振结构式
共振式书写七条规则
- 只移动电子,不移动原子(原子骨架不变)
- 每个共振式都必须是合理的Lewis结构
- 各共振式未成对电子数必须相同
- 共价键越多的共振式越稳定(贡献越大)
- 所有原子都满足八隅体的更稳定
- 电荷分离越少的越稳定
- 负电荷在电负性大的原子上更稳定
共振≠互变异构:共振结构式是同一分子的不同电子描述(不能独立存在),真实结构是各共振式的杂化体。互变异构是不同分子的平衡。
判断共振式贡献大小:满足上述规则4-7越多的共振式贡献越大。无电荷分离 > 有电荷分离;满足八隅体 > 不满足。
2.2b 共轭二烯烃与共轭效应
丁-1,3-二烯的结构特征
丁-1,3-二烯中4个碳均为sp2杂化,4个p轨道相互平行重叠形成大π键(离域π键)。
- C2−C3键长:146.0 pm,介于C−C单键(154 pm)和C=C双键(134 pm)之间 → 键长平均化
- 分子近乎平面构型,电子离域在整个共轭体系上
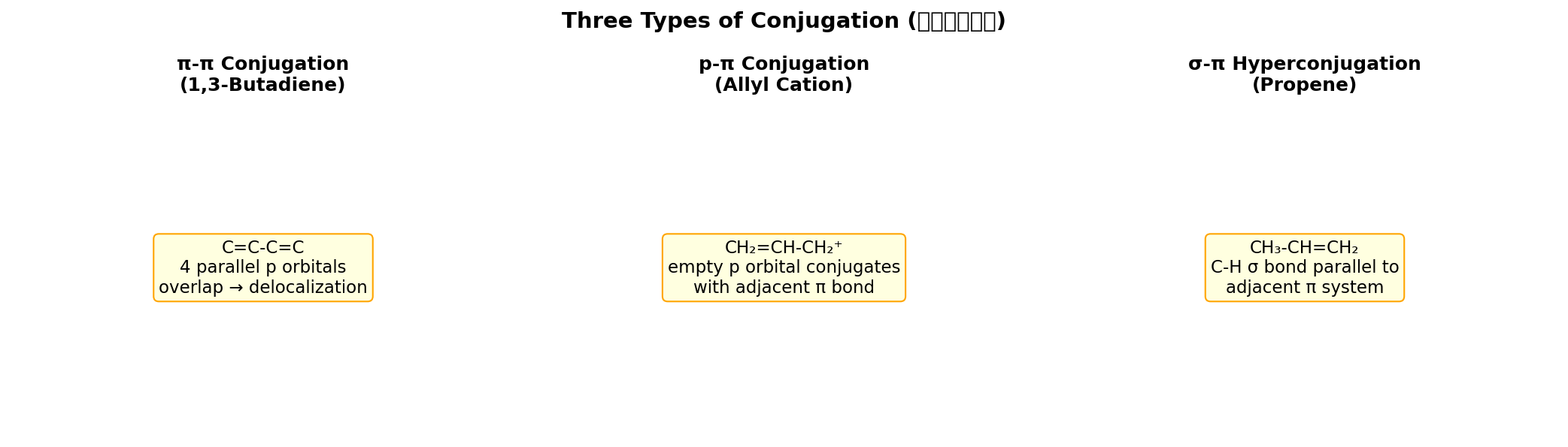
共轭效应(离域效应)
定义:在共轭体系中,电子离域(不再局限于两个原子之间)导致体系能量降低、稳定性增大的效应。
氢化热数据验证:
| 化合物 | 氢化热/(kJ/mol) | 说明 |
|---|
| 1-丁烯(一个C=C) | 127 | 基准值 |
| 1,4-戊二烯(孤立二烯) | 254(≈127×2) | 无共轭稳定化 |
| 1,3-丁二烯(共轭二烯) | 237 | 比预期(254)低约17 kJ/mol |
差值(~17 kJ/mol)即为共轭稳定化能。
HOMO与LUMO简介
- HOMO(最高占据分子轨道):含有电子的能量最高的分子轨道,决定分子给出电子的能力
- LUMO(最低未占据分子轨道):不含电子的能量最低的分子轨道,决定分子接受电子的能力
- HOMO-LUMO能量差越小,分子越容易发生反应
2.3 不饱和度(DBE)
不饱和度计算公式
$$\text{DBE} = \frac{2C + 2 + N - H - X}{2}$$
C=碳数,N=氮数,H=氢数,X=卤素数。O和S不参与计算。
不饱和度的含义:
DBE=0 → 饱和(烷烃/醚等)
DBE=1 → 1个双键或1个环
DBE=2 → 2个双键/环或1个三键
DBE=4 → 很可能含苯环(3双键+1环)
例:C7H6O2 的DBE = (2×7+2-6)/2 = 5。含苯环(4)+1个C=O或环。
2.4 IUPAC系统命名法
命名四步法
- 选主链:含官能团(双/三键)的最长碳链;同长选取代基最多的
- 编号:使取代基位次之和最小(最低位次组规则);有双/三键时让不饱和键编号最小
- 命名取代基:按英文字母顺序排列(ethyl > methyl)
- 组合:位次-取代基名称-母体名(烷/烯/炔)
碳的分类
| 类型 | 连接C数 | 符号 | 氢叫法 |
|---|
| 伯碳 | 1个C | 1° | 伯氢 |
| 仲碳 | 2个C | 2° | 仲氢 |
| 叔碳 | 3个C | 3° | 叔氢 |
| 季碳 | 4个C | 4° | 无氢 |
命名实例:
CH3CH(CH3)CH2CH2CH3 → 2-甲基戊烷
(CH3)3CCH2CH(CH3)2 → 2,2,4-三甲基戊烷
CH3CH=CHCH2CH3 → 2-戊烯
烯基命名
| 中文名 | 英文名 | 结构 |
|---|
| 乙烯基 | vinyl / ethenyl | CH2=CH− |
| 丙烯基 | propenyl | CH3CH=CH− |
| 烯丙基 | allyl / 2-propenyl | CH2=CHCH2− |
| 异丙烯基 | isopropenyl | CH2=C(CH3)− |
注意区分:丙烯基(双键在1,2位,取代在1位)vs 烯丙基(双键在1,2位,取代在3位)。
复杂支链命名
当支链本身还有支链(取代基上有取代基)时:
- 支链名称用括号括起来
- 支链编号从与主链直接相连的碳开始(而非从支链端头)
- 例:主链上连有 −CH(CH3)CH2CH3,从连接点编号 → 1-甲基丙基,写作 (1-甲基丙基)
2.5 环烃命名
单环命名
环+碳数+烷/烯/炔。如:环己烷、环戊烯、1,3-环己二烯
取代环烃:取代基少 → 环为母体;取代基多或链长 → 链为母体+环为取代基
桥环命名
二环[a.b.c]某烷:a≥b≥c,a、b、c为三座桥的碳数(不包含桥头碳)
编号:从一个桥头碳开始,沿最长桥→次长桥→最短桥编号
实例详解:
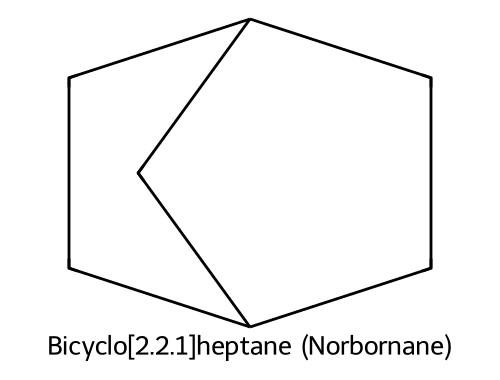
- 降冰片烷 = 二环[2.2.1]庚烷:共7个碳,两个桥头碳 + 三座桥分别含2、2、1个碳(2+2+1+2桥头=7)
- 二环[3.3.1]壬烷:共9个碳,三座桥分别含3、3、1个碳(3+3+1+2桥头=9)
- 二环[2.2.2]辛烷:共8个碳,三座桥各含2个碳(2+2+2+2桥头=8)
螺环命名
螺[a.b]某烷:a≤b,a和b分别为两个环中不包括螺原子的碳数
编号:从小环上与螺原子相邻的碳开始编号,绕小环→经螺原子→绕大环
实例详解:
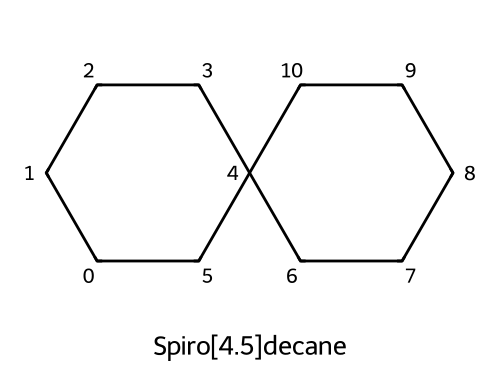
- 螺[4.5]癸烷:总碳数=4+5+1(螺原子)=10(癸=10碳)。[4.5]表示小环除螺原子外有4个碳,大环除螺原子外有5个碳。即一个五元环和一个六元环共享一个螺原子。
- 螺[3.4]辛烷:总碳数=3+4+1=8。一个四元环和一个五元环共享螺原子。
- 螺[2.5]辛烷:总碳数=2+5+1=8。一个三元环和一个六元环共享螺原子。
桥环实例:降冰片烷 = 二环[2.2.1]庚烷(共7个碳,桥分别含2、2、1个碳)
2.6 Z/E命名与CIP规则
CIP次序规则(Cahn-Ingold-Prelog)
- 原子序数大者优先:I > Br > Cl > S > O > N > C > H
- 同种原子时逐层外推比较:沿链向外逐个比较直到分出高低
- 双键/三键拆分处理:C=C当作每个C各连一个"虚原子C"
- 质量数大的同位素优先:D(²H) > H(¹H)
Z/E判断
对双键两端各选优先级高的基团:
两个高优先基团在同侧 = Z(zusammen),异侧 = E(entgegen)
Z/E ≠ 顺/反(cis/trans):
顺/反是按相同基团判断,Z/E按CIP次序规则判断。例:
(Z)-1-溴-1-氯-2-碘乙烯中,Br和I同侧为Z,但按传统顺反可能称为反式。
烯炔共存时:先烯后炔命名(-X-烯-Y-炔);同位次时双键编号优先于三键。
顺反异构体不存在的条件:当双键某一端的两个基团相同时(如 CH2=CHR 或 R2C=CR'R''中一端为RR),该分子没有顺反异构体(Z/E构型无意义)。必须双键两端各连两个不同基团才有顺反异构。
2.7 常见官能团与分类
| 官能团 | 结构 | 化合物类 | 命名后缀 |
|---|
| 碳碳双键 | C=C | 烯烃 | -烯(-ene) |
| 碳碳三键 | C≡C | 炔烃 | -炔(-yne) |
| 羟基 | −OH | 醇 | -醇(-ol) |
| 醚键 | −O− | 醚 | -醚(ether) |
| 醛基 | −CHO | 醛 | -醛(-al) |
| 酮基 | −CO− | 酮 | -酮(-one) |
| 羧基 | −COOH | 羧酸 | -酸(-oic acid) |
| 酯基 | −COOR | 酯 | -酸某酯(-oate) |
| 氨基 | −NH2 | 胺 | -胺(-amine) |
| 酰胺基 | −CONH2 | 酰胺 | -酰胺(-amide) |
| 卤素 | −X | 卤代烃 | 卤代-(halo-) |
课后习题精选
题1 杂化态判断
题1 判断下列化合物中每个C、N、O原子的杂化态:
(a) CH2=CHCHO
(b) CH3CN
(c) CH2=C=CH2(丙二烯)
(d) HCONH2(甲酰胺)
解题思路:σ键数+孤电子对数=杂化轨道数。2=sp,3=sp2,4=sp3。参与π键的孤电子对不计入(p-π共轭)。
(a) CH2=CHCHO(丙烯醛):
| 原子 | σ键数 | 孤电子对(杂化) | 杂化 | 理由 |
|---|
| C1(=CH2) | 3 | 0 | sp2 | 形成C=C双键 |
| C2(=CH) | 3 | 0 | sp2 | 形成C=C双键 |
| C3(=O) | 3 | 0 | sp2 | 形成C=O双键 |
| O | 1 | 2 | sp2 | 一对孤电子参与p-π共轭(与C=O共面) |
整个分子共面,形成贯穿全分子的π共轭体系(π-π共轭)。
(b) CH3CN(乙腈):
| 原子 | σ键数 | 孤电子对(杂化) | 杂化 |
|---|
| C(CH3) | 4 | 0 | sp3 |
| C(≡N) | 2 | 0 | sp |
| N | 1 | 1 | sp |
C≡N为直线形,N的一对孤电子占据sp杂化轨道(沿轴方向伸出)。
(c) CH2=C=CH2(丙二烯 allene):
| 原子 | 杂化 | 说明 |
|---|
| C1, C3 | sp2 | 各形成一个C=C |
| C2(中心) | sp | 形成两个C=C双键,两个π键互相垂直 |
重点:中心碳为sp杂化!两端CH2平面互相垂直(90°二面角)。这导致丙二烯具有轴手性(当两端取代基不同时为手性分子)。
(d) HCONH2(甲酰胺):
| 原子 | 杂化 | 说明 |
|---|
| C | sp2 | 形成C=O双键 |
| O | sp2 | C=O中的O |
| N | sp2 | N的孤电子对与C=O形成p-π共轭(酰胺共振) |
酰胺N为sp2而非sp3!这是因为N的孤电子对参与共振:H2N-C=O ↔ H2N+=C-O−。所以酰胺键是平面的(蛋白质肽键的基础)。
题2 不饱和度(DBE)
题2 计算不饱和度并推测可能结构:
(a) C8H8
(b) C4H6O
(c) C6H5NO2
(d) C3H5ClO
解题思路:DBE = (2C+2+N−H−X)/2。O、S不影响计算。DBE≥4考虑苯环(=4)。
(a) C8H8:DBE = (2×8+2−8)/2 = 5
5 = 苯环(4) + 1个双键或环。可能结构:苯乙烯 C6H5CH=CH2(最合理)、环辛四烯(全顺式4个双键+1环=5,也符合)。
(b) C4H6O:DBE = (2×4+2−6)/2 = 2
2个不饱和度。可能:丁烯醛 CH3CH=CHCHO(1 C=C + 1 C=O)、甲基乙烯基酮 CH3COCH=CH2、环丙基甲醛(1环+1 C=O)。
(c) C6H5NO2:DBE = (2×6+2+1−5)/2 = 5
5 = 苯环(4) + 1。→ 硝基苯 C6H5NO2(硝基中N=O贡献1个不饱和度)。
(d) C3H5ClO:DBE = (2×3+2−5−1)/2 = 1
1个不饱和度。可能:环氧氯丙烷(环氧环=1)、3-氯丙醛 ClCH2CH2CHO(C=O=1)、氯丙酮 CH3COCH2Cl。
卤素X当作H处理(减1个H当量);N加1个H当量。O、S不参与计算。
题3 IUPAC命名
题3 对下列化合物进行IUPAC系统命名:
(a) (CH
3)
2CHCH
2C(CH
3)
2CH
2CH(C
2H
5)CH
3
(b) (E)-3-甲基-4-异丙基-3-庚烯(验证E/Z标定)
(c)
![螺[4.5]癸烷](img/naming_spiro45decane.png)
螺环化合物
(d)
![双环[2.2.1]庚烷](img/naming_norbornane.png)
桥环化合物
(e) CH
3CH=C(CH
3)CH
2CH(OH)CH
3
(f) (CH
3)
3CCH
2CH(CH
3)CH
2CH
3
解题思路:①找最长碳链(含官能团)②编号使取代基位次最小 ③先列取代基(按字母序或复杂度)④标E/Z或R/S。
(a) 展开:C-C(C)-C-C(C)(C)-C-C(C2H5)-C
最长链8C:2,4,4,6-四甲基-6-乙基辛烷 → 不对。重新数:主链为C1-C2-C3-C4-C5-C6-C7-C8。
答:2,4,4-三甲基-6-乙基辛烷
(b) 主链7C(庚),3位甲基,4位异丙基,双键在3位。判断E/Z:C3双键碳上 → 高优先级侧为主链(C4-C7) vs CH3;C4双键碳上 → (CH3)2CH vs 主链(C5-C7)。两个高优先级基团在异侧 → (E)-4-异丙基-3-甲基-3-庚烯
(c) 螺环:两个环共享一个碳原子。环大小=4+5碳(不含共享碳)=9个碳+共享碳=10碳。
答:螺[4.5]癸烷(spiro[4.5]decane)
编号:从小环邻接螺原子开始,先经小环再经大环。
(d) 桥环:两个环共享两个碳(桥头碳)。总碳数=7。三条桥分别为2C、2C、1C。
答:双环[2.2.1]庚烷(bicyclo[2.2.1]heptane,即降冰片烷norbornane)
编号:从一个桥头碳开始,先沿最长桥→另一桥头→次长桥返回→最短桥。
(e) 含OH优先。最长含C=C和OH的链为6C。OH在5位,C=C在2位。
答:3-甲基-2-己烯-5-醇(或按新规 3-methylhex-2-en-5-ol)
(f) 新戊基型。最长链6C。
答:2,2,4-三甲基己烷
题4 由名称写结构
题4 写出下列化合物的结构式:
(a) (2E,4Z)-2,4-己二烯
(b) 螺[3.4]辛-1-烯
(c) 7-甲基双环[2.2.1]庚-2-烯
(d) (R)-3-氯-1-丁烯
解题思路:先画碳骨架→标双键位置→确定几何/立体构型。
(a) (2E,4Z)-2,4-己二烯:6碳链,C2=C3和C4=C5双键。
C2=C3:两个高优先级基团(C1H3在C2, C4链在C3)分居两侧→E。
C4=C5:高优先级基团(C3链在C4, C6H3在C5)分居同侧→Z。
结构:CH3\C=C/H 且 H\C=C/CH3(中间连接)→ CH3-CH=CH-CH=CH-CH3,2位E构型3位Z构型。
(b) 螺[3.4]辛-1-烯:螺环,小环4碳环,大环5碳环,共享螺原子=总8碳。从小环邻螺碳编号,C1=C2有双键。
(c) 7-甲基双环[2.2.1]庚-2-烯:降冰片烯骨架,C7(单碳桥上)连甲基,C2=C3双键。
(d) (R)-3-氯-1-丁烯:CH2=CH-CHCl-CH3。C3为手性碳(连H, Cl, CH=CH2, CH3)。
CIP优先级:Cl > CH=CH2 > CH3 > H。H在后方时,Cl→乙烯基→甲基为顺时针→R构型。
题5 共振结构
题5 画出所有重要共振结构并排列贡献大小:
(a) 烯丙基碳正离子 CH2=CH−CH2+
(b) 乙烯基胺 CH2=CH−NH2(p-π共轭)
(c) 1,3-丁二烯 CH2=CH−CH=CH2(π-π共轭)
解题思路:共振结构书写规则——只移动电子(π或孤电子对),不移动原子。贡献排序:①满足八隅体 ②电荷分离少 ③负电在电负性大原子上。
(a) 烯丙基碳正离子(p-π共轭:空p轨道与π键共轭):
I: CH2=CH−CH2+ ←→ II: +CH2−CH=CH2
两个共振式完全等价,贡献相同。正电荷平均分布在C1和C3上(各+0.5),C2不带电荷但参与π体系。键长:C1-C2 = C2-C3 ≈ 1.38 Å(介于单双键之间)。
(b) 乙烯基胺 CH2=CH−NH2(p-π共轭:N孤电子对与C=C共轭):
I: CH2=CH−NH2 ←→ II: −CH2−CH=NH2+
贡献:I > II。理由:II有电荷分离(不利),且N上正电荷不利(N电负性大)。
但II说明:①N的碱性降低(孤电子对部分离域)②C1有部分负电荷(亲电加成的位点)③C-N键有部分双键性质(旋转受阻)。
这正是酰胺和烯胺中N碱性低于普通胺的原因——孤电子对参与共轭离域。
(c) 1,3-丁二烯(π-π共轭):
I: CH2=CH−CH=CH2(主要)
II: +CH2−CH=CH−CH2−(次要)
III: −CH2−CH=CH−CH2+(次要,与II等价)
贡献:I ≫ II = III。I无电荷分离贡献最大。II和III说明C2-C3有部分双键性质(旋转势垒约25 kJ/mol),C1和C4有微弱的负/正电荷倾向。
题6 CIP优先级排序
题6 按CIP规则排列优先级(从高到低):
(a) −CH3, −CH2OH, −CHO, −CH=CH2
(b) −C≡CH, −CH=CH2, −CH2CH3, −C(CH3)3
(c) −Cl, −CH2Cl, −CCl3, −CHCl2
解题思路:逐层比较。关键规则——双键/三键的"虚原子"展开:C=C展开为C连(C,C,...),C≡C展开为C连(C,C,C)。
(a) 第一层原子:全是C,需看第二层。
| 基团 | 中心C连接 | 第二层 |
|---|
| −CHO | H, =O → 展开(H, O, O) | (O,O,H) |
| −CH=CH2 | H, =C → 展开(H, C, C) | (C,C,H) |
| −CH2OH | H, H, O | (O,H,H) |
| −CH3 | H, H, H | (H,H,H) |
比较第二层最高原子:O > C > O(但配对不同) > H
答:−CHO > −CH2OH > −CH=CH2 > −CH3
注意−CHO中C的展开:C=O → C连接(O,O,H),两个O中一个是虚原子。−CH2OH的第二层是(O,H,H)。比较时:CHO的(O,O,H) vs CH2OH的(O,H,H)→第一个O相同,第二位O>H,所以CHO优先。
(b) 虚原子展开:
| 基团 | 展开后第一个C连接 |
|---|
| −C≡CH | (C,C,C) — 三键展开3个虚C |
| −CH=CH2 | (C,C,H) — 双键展开2个虚C |
| −C(CH3)3 | (C,C,C) — 3个真实C |
| −CH2CH3 | (C,H,H) |
−C≡CH vs −C(CH3)3:第二层都是(C,C,C),继续到第三层。−C≡CH的虚C没有进一步连接(原子序数=0),−C(CH3)3的每个C连3个H。真实原子>虚原子?不,CIP规则中虚原子的原子序数与真实原子相同!需进一步比较。
实际上:−C(CH3)3第三层每个C→(H,H,H);−C≡CH第三层虚C→(C,C,C原子序数为6但无后续)。规则:虚原子只有原子序数,无后续取代基。
答:−C≡CH > −C(CH3)3 > −CH=CH2 > −CH2CH3
(c) 第一层原子:Cl(直接连) vs C(其余三个)。
−Cl:第一层直接就是Cl(17) → 最高优先级。
其余比较第二层:−CCl3(Cl,Cl,Cl) > −CHCl2(Cl,Cl,H) > −CH2Cl(Cl,H,H)。
答:−Cl > −CCl3 > −CHCl2 > −CH2Cl
题7 综合命名实战
题7 给出下列复杂化合物的完整IUPAC名称(含立体标识):
(a) CH3CH=C(Cl)CH2CH(CH3)CH2OH
(b) 分子式C10H16的双环[2.2.2]辛烷衍生物,1,4位各连甲基
(c) (2R,3S)-2-氯-3-甲基戊酸
解题思路:①确定主官能团(醇>烯>卤)②选含主官能团最长链 ③编号使主官能团位次最小 ④标立体。
(a) 主官能团=OH(醇)。含OH和C=C最长链=6C(己)。OH在C1→编号从OH端开始。
C1: CH2OH, C2: CH(CH3), C3: CH2, C4: C(Cl)=, C5: CH=, C6: CH3
名称:4-氯-2-甲基-4-己烯-1-醇
E/Z判断:C4连Cl和C3链,C5连C6(CH3)和H。C4高优先=Cl,C5高优先=CH3→同侧=Z。
答:(Z)-4-氯-2-甲基-4-己烯-1-醇
(b) 双环[2.2.2]辛烷有8C,加2个CH3=C10H16(验证:C8H14+2CH2=C10H18? 不对。双环[2.2.2]辛烷=C8H14,加2个甲基→C10H18。题目说C10H16,DBE=3=双环(2)+1双键。所以含一个双键。
答:1,4-二甲基双环[2.2.2]辛-2-烯
(c) 戊酸=5C链+COOH。C2连Cl(R构型),C3连CH3(S构型)。
答:(2R,3S)-2-氯-3-甲基戊酸(即题目本身就是名称,验证:主链5C含COOH,C2-Cl,C3-CH3,两个手性中心分别为R和S→这是赤式/苏式异构体之一)。



![螺[4.5]癸烷](img/naming_spiro45decane.png) 螺环化合物
螺环化合物![双环[2.2.1]庚烷](img/naming_norbornane.png) 桥环化合物
桥环化合物